Эбулиоскопический метод
Cтраница 3
При определении молекулярного веса вещества как по повышению температуры кипения ( эбулиоскопический метод), так и по понижению температуры замерзания ( криоскопический метод) необходимо применять особо чувствительный термометр - термометр Бекмана, позволяющий производить отсчеты температуры с точностью не меньшей, чем 0 005 С. [31]
При определении молекулярного веса вещества как по повышению температуры кипения ( эбулиоскопический метод), так и по понижению температуры замерзания ( крирскопический метод) необходимо применять особо чувствительный термометр - термометр Бекмана, позволяющий производить отсчеты температуры с точностью не меньшей, чем 0 005 С. [32]
Формула обоснована определением молекулярного веса эфирата, полученного из йодистого метила, эбулиоскопическим методом. Оказалось, что эфират имеет удвоенный молекулярный вес. Существование координационных связей эфира с атомом магния подтверждают и последние данные по исследованию сольватации в эфирных растворах реактивов Гриньяра методом инфракрасных спектров. При электролизе реактива Гриньяра на катоде отлагается магний в половинном количестве, что также свидетельствует в пользу приведенной формулы. [33]
Формула обоснована определением молекулярного веса эфирата, полученного из йодистого метила, эбулиоскопическим методом. Оказалось, что эфират имеет удвоенный молекулярный вес. [34]
Формула обоснована определением молекулярного веса эфирата, полученного из йодистого метила, эбулиоскопическим методом. Оказалось, что-эфират имеет удвоенный молекулярный вес. [35]
 |
Принципиальная схема эбулиометра. [36] |
Какой из растворителей: ацетон, бензол или хлороформ - наиболее пригоден для определения молекулярной массы поливинилацетата эбулиоскопическим методом. [37]
В табл. 4 приведены максимальные значения молекулярного веса, рассчитанные по формуле ( 10), которые могут быть найдены крио-скопическим или эбулиоскопическим методом при разных истинных значениях среднечислового молекулярного веса полимера ( AQ и при содержании воды 0 1 и 1 0 вес. [38]
Изучение температур кипения растворов и параллельное исследование давления их паров ( см. ниже) в конечном итоге привели к созданию ( 1890) эбулиоскопического метода определения молекулярных весов. [39]
Впервые такой прием оценки отклонения от аддитивности был предложен Урбаном и Вурионом и использован в работах Буриона и Ройера по исследованию комплексообра-зования в водных растворах электролитов преимущественно эбулиоскопическим методом. [40]
Возможность перегруппировок, которые в некоторых условиях: оказываются обратимыми, должна всегда приниматься во внимание при физических измерениях, например при определении молекулярного веса, органического вещества эбулиоскопическим методом в растворе фтористого водорода. [41]
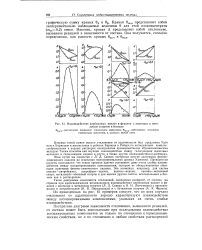 |
Взаимодействие карбоновых кислот и фенолов с ацетоном и метиловым спиртом в бензоле. [42] |
Впервые такой, прием оценки отклонения от аддитивности был предложен Урба ом и Бурионом и использован в работах Буриона и Ройера по исследованию комплек-сообразования в водных растворах электролитов преимущественно эбулиоскопическим методом. [43]
Следует отметить, что принципиально среднечисловые молекулярные веса получаются при измерении с помощью любого термодинамического метода - по понижению температуры замерзания растворителя ( криоскопический метод), по повышению температуры кипения растворителя ( эбулиоскопический метод), по давлению пара растворителя над раствором, по равновесному распределению макромолекул в силовом поле ( седиментационное равновесие) и др. Однако каждый из этих методов имеет свои специфические источники ошибок при измерениях, и поэтому результаты не всегда сходятся. Так, например, ничтожно малое количество низкомолекулярной примеси может вызвать весьма заметное понижение среднего значения молекулярного веса при криоскопическом измерении и мало влияет на результаты, полученные осмометрическим методом. [44]
Так как несоответствие молекулярных весов, вычисленных на основании ( вообще очень точного) криоскопического метода, с истинными весами выражалось всегда отношением, указывавшим на то, что вычисленные веса меньше истинных, и так как для каждого данного случая точно такие же результаты давали эбулиоскопический метод и исследование осмотического давления, то Аррениус, решительно отвергнув мысль о возможности - ошибок эксперимента, с уверенностью заключил отсюда, что электролитические растворы действительно имеют средний молекулярный вес, меньший должного. Сопоставив этот вывод с поведением электролитов при прохождении через них тока, Аррениус нашел, что синтез ионной теории Фарадея с теорией растворов устраняет многие трудности в объяснении явлений электролиза и других электрохимических явлений. Действительно, камнем преткновения в Фарадеевской теории была причина распада молекул на ионы; теперь же с очевидностью обнаружилось, что было бы лишним искать эту причину в разности потенциалов на электродах ( как то делал Фарадей) или в столкновении молекул ( чем стремился исправить Фара-дееву теорию Клаузиус); стало ясно, что причина эта коренится в самой природе электролитов, она является той особенностью их, которая отличает их от обыкновенных растворов. [45]
Страницы: 1 2 3 4