Аммин
Cтраница 3
Преимуществами растворов КАС перед растворами амминов ( аммиакатов) и жидким аммиаком является отсутствие потерь азота вследствие очень малого содержания летучего аммиака, возможность хранения и транспортировки в резервуарах и цистернах, изготовленных из дешевой углеродистой стали и не рассчитанных на повышенное давление, более простые приемы внесения в почву, в частности с использованием авиации. [31]
Необходимость присутствия воды для образования аммина проявляется и в отношении фтористого кобальта к пиридину. [32]
Бьеррум Я -, Образование амминов металлов в водном растворе. [33]
АММИАКАТЫ, то же, что аммины. [34]
Значения обычно неизвестны, но для амминов и комплексов с аминами они, как правило, имеют порядок 10 - 14, так как при 25 / ГН2О10 - и. Поэтому величины / с, приведенные в табл. 24, оказываются равными / сщел. [35]
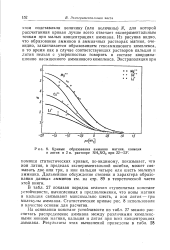 |
Кривые образования амминов магния, кальция и лития в 2 н. растворе NH4NO3 при 22 - 23. [36] |
Из рисунка видно, что образование амминов в аммиачных растворах магния, очевидно, заканчивается образованием гексамминового комплекса, в то время как в случае соответствующих растворов кальция и лития нельзя с уверенностью говорить о составе координационно насыщенного амминового комплекса. [37]
Из таблицы ясно, что образование амминов происходит настолько слабо, что неисправленные значения функции образования даже несколько отрицательны. Исправленные значения, по-видимому, показывают, что константа устойчивости, которую Жоб вычислил для комплекса моноамминталлия ( I), имеет правильный порядок величины. [38]
Исследование сильно облегчается, если образование амминов начинается при достаточно малой концентрации ионов гид-роксила, когда гидроксо-соединения образуются лишь в незначительных количествах. В большинстве случаев такое условие выполняется при достаточно высокой концентрации ионов аммония. Если акво-ионы металла имеют явно кислотный характер, необходимо принимать во внимание образование гидроксо-соединений. Для большинства одно - и двухзарядных ионов металлов кислотный характер не имеет большого значения. Однако кислотный характер трехзарядных ионов настолько ярко выражен, что гидроксо-соединения образуются в больших количествах, вследствие чего исследование образования амминов обычно становится невозможным. Кроме того, в отдельных случаях необходимо учитывать образование амидо-комплексов, например в системах аммиачных комплексов ртути и платины. [39]
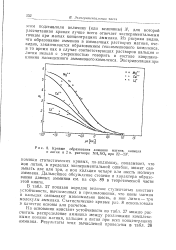 |
Кривые образования амминов магния, кальция и лития в 2 н. растворе NH4NO3 при 22 - 23. [40] |
Из рисунка видно, что образование амминов в аммиачных растворах магния, очевидно, заканчивается образованием гексамминового комплекса, в то время как в случае соответствующих растворов кальция и лития нельзя с уверенностью говорить о составе координационно насыщенного амминового комплекса. [41]
Из таблицы ясно, что образование амминов происходит настолько слабо, что неисправленные значения функции образования даже несколько отрицательны. Исправленные значения, по-видимому, показывают, что константа устойчивости, которую Жоб вычислил для комплекса моноамминталлия ( I), имеет правильный порядок величины. [42]
Здесь, как и в случае амминов меди ( II), найденное семейство кривых позволяет сделать вывод, что происходит только чистое образование амминов металлов. [43]
 |
Поляризационная схема трансвлияния по Гринбергу - Некрасову. [44] |
С другой стороны, заменив аммиак органическим аммином, мы не получим практически никакого изменения в способности данного лиганда к трансвлиянию, тогда как рефракция амина может стать сколько угодно большой. Значит, сама по себе рефракция лиганда не может служить количественной характеристикой трансвлияния. [45]
Страницы: 1 2 3 4