Микромоль
Cтраница 3
Одна единица ( Е) любого фермента представляет то количество фермента, которое при заданных условиях катализирует превращение одного микромоля субстрата в одну минуту или одного микроэквивалента затронутой группы в тех случаях, когда атакуется более одной группы в каждой молекуле субстрата. Прочие условия, в частности рН и концентрации субстратов, должны быть по возможности оптимальными; в случаях несоблюдения упомянутых условий это должно быть ясно оговорено. [31]
Реакцию регистрируют 1 - 2 мин, чувствительность прибора калибруют внесением титрованного раствора НС1 и рассчитывают удельную активность в микромолях АДФ, превращенного за 1 мин в расчете на 1 мг белка. [32]
Активность очищенных и обогащенных препаратов в большинстве случаев выражают в микромолях ацетилхолина на 1 мг сухого вещества или, после определения белка по способу Кьельдаля, в микромолях ацетилхолина на 1 мг белка в час. [33]
Для определения активности нитратредуктазы в полученных ферментных препаратах в стеклянные центрифужные пробирки емкостью около 10 мл помещают 20 микромолей ( 0 2 мл 0 1 М раствора) KNO3, 0 2 микромоля НАД-Н2 или НАДФ-Н2 ( растворы с концентрацией 4 - 5 микромолей), 1 7 мц М ФАД ( 0 1 мл 1 7 - 16 - 5 миллимолярного раствора), 0 5 мл ферментного препарата и 0 15 М фосфатный буфер с рН 7 0 до конечного объема 1 мл. Инкубацию системы проводят в термостате при температуре 28 в течение 15 - 30 минут. В конце инкубационного периода к реакционной смеси на холоде прибавляют 0 2 мл 1 М раствора ацетата бария и 5 мл 95 - 97 % - ного этанола. Небольшой осадок белка отделяют центрифугированием. В центрифугате определяют нитриты. [34]
Расчет активности фермента во всех случаях проводят на основании величин начальной скорости реакции при условии наличия прямой пропорциональной зависимости скорости реакции от количества ферментного препарата в пробе, Скорость фермента выражают в микромолях превращенных субстратов за 1 мин на 1 мг микросомального белка или на 1 г ткани. [35]
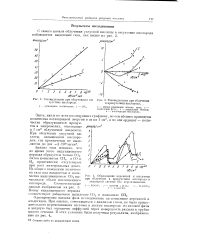 |
Газовыделеиие при облучении в отсутствие кислорода.| Газовыделение при облучении в присутствии кислорода.. [36] |
Здесь, как и во всех последующих графиках, по оси абсцисс приведены количества поглощенной энергии в эв на 1 см3, а по оси ординат - количества образующихся продук - 3 тов в микромолях, отнесенные fJMOJib / см к 1 см3 облучаемой жидкости. [37]
Расчет количества малонового диальдегида ( ТБК-позитивных веществ) производят по формуле: С Л532 / М, где Л532 - оптическая плотность пробы; М - молярный коэффициент экстинкции, равный 1 56 105 моль - 1см - 1; С - концентрация МДА ( ТБК-позитивных веществ), выраженная в микромолях на 1 мл плазмы или микромолях на 1 мл эритроцитарной массы. В физиологических условиях концентрация МДА в плазме крови составляет 0 82410 0389 мкмоль / мл, в эритроцитах - 8 353 0 300 мкмоль / мл. [38]
Расчет количества малонового диальдегида ( ТБК-позитивных веществ) производят по формуле: С Л532 / М, где Л532 - оптическая плотность пробы; М - молярный коэффициент экстинкции, равный 1 56 105 моль - 1см - 1; С - концентрация МДА ( ТБК-позитивных веществ), выраженная в микромолях на 1 мл плазмы или микромолях на 1 мл эритроцитарной массы. В физиологических условиях концентрация МДА в плазме крови составляет 0 82410 0389 мкмоль / мл, в эритроцитах - 8 353 0 300 мкмоль / мл. [39]
В течение малого периода индукции TJTT наступает самовоспламенение в результате превышения тепловыделения в микрообъеме над теплоотводом с его поверхности. В микромолях с неблагоприятными температурными и концентрационными условиями реакции слаба развиваются, или они, не успев воспламениться в течение малого периода индукции, вступают в последующее смешение. Таким образом распространение турбулентного пламени представляется как пульсирующее самовоспламенение микрообъемов. [40]
Расчет активности фермента проводят на основании величин начальной скорости реакции при условии наличия прямой пропорциональной зависимости скорости реакции от количества ферментного препарата в пробе. Активность фермента выражают в микромолях окисленного НАДН за 1 мин на 1 г ткани. [41]
Расчет активности фермента проводят на основании величин начальной скорости реакции при условии наличия прямой пропорциональной зависимости скорости реакции от количества ферментного препарата в пробе. Активность фермента выражают в микромолях восстановленного НАДФ за 1 мин на 1 г ткани. [42]
Расчет активности фермента проводят на основании величин начальной скорости реакции при условии наличия прямой пропорциональной зависимости скорости от количества ферментного препарата в пробе. Скорость гексокнназы выражают в микромолях восстановленного НАДФ в мин. [43]
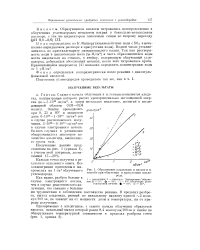 |
Образование альдегидов и кислот в н. гептане при облучении в присутствии кислорода. [44] |
Каждая точка получена в результате отдельного опыта. Все концентрации приведены в микромолях на 1 см3 облученного углеводорода. [45]
Страницы: 1 2 3 4