Микротом
Cтраница 4
Приготовленные таким образом пробы под слоем парафина в микротоме разрезают на пластинки толщиной 5 мм, парафин экстрагируют 50 мл гексана. [46]
Для этого из образцов пенополистирола вручную или на специальных микротомах изготавливают срезы толщиной 10 - 15 мкм, которые просматривают под микроскопом в проходящем свете. При изготовлении срезов вручную ( при помощи лезвия) не требуется предварительной подготовки пенополистирола. При изготовлении срезов на микротоме образцы пенополиетирола предварительно обрабатывают для получения плотной, хорошо режущей массы: парафинируют или желатинизируют, после чего замораживают. Для парафинирования образцы разогревают, поэтому обрабатывать таким способом можно пенополистирол с теплостойкостью выше 70 G. Готовые срезы хорошо сохраняются в воде. [47]
 |
Держатель образца для резки с замораживанием, смонтированный на ротационном микротоме типа Портера - Блюма. [48] |
Метод замораживания образца для приготовления срезов вулка-низатов на микротоме ротационного типа был описан Чепиусом и Робблсом 1В в 1957 г. Они поддерживали образец в замороженном состоянии при микротомировании при помощи смеси сухого льда и спирта. Замораживание образца жидким азотом11 с использованием ротационного микротома типа Портера - Блюма, также позволяет изготовлять срезы высокого качества, достаточно тонкие для исследования в электронном микроскопе. [49]
Уже с начала сороковых годов неоднократно предпринимались попытки применить микротомы для получения достаточно тонких срезов препаратов, пригодных для изучения в электронном микроскопе. Предложенные вначале различные варианты конструкций микротомов, в том числе основанные на быстром вращении ножа, оказались недостаточно эффективными. [50]
 |
Нож с ванночкой. [51] |
Подготовленный для резания блок полимера помещают в держатель образцов микротома. Держатель образцов закрепляют в гнезде гониометрического устройства с помощью зажимного винта. Стеклянный нож закрепляют в держателе ножа так, чтобы передняя грань ножа была бы расположена вертикально к плоскости основания прибора. Затем, освободив зажимной винт держателя ножа и поворачивая его, устанавливают нож так, чтобы его передняя грань составляла с вертикалью угол 3 - 4, а лезвие ножа располагалось параллельно одной из граней пирамиды. Медленно вращая микроподачу, производят срез. Полученный срез осторожно снимают препаратор-ной иглой и помещают между двумя предметными стеклами. После этого распрямленный срез обрабатывают контрастирующей жидкостью К2 ( HgI4), закрывают покровным стеклом и помещают на предметный столик микроскопа для исследования. Толщина срезов не должна превышать 2 - 3 мкм. [52]
В стационарных условиях клиники или научно-исследовательского института охлаждающий столик микротома может получать питание от обычной осветительной сети через типовой селеновый выпрямитель ВСА-10. [53]
После работы на микрогаме необходимо сразу же вынимать из микротома нож и помещать его в футляр для постоянного хранения. Оставлять нож в микротоме или переносить его без футляра по лаборатории запрещается. [54]
Лучшие результаты получают при работе ео срезами, изготовленными на замораживающем микротоме, так как удается избежать отрицательного действия спирта, ксилола и нагревания на связь РНК с липидами во время пропитывания объекта парафином. [55]
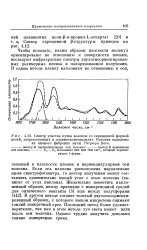 |
Спектр участка пучка волокон со скрещенной формой. [56] |
В другом методе готовят толстый двухосноориенти-рованный образец, с которого ножом микротома снимают тонкий поперечный срез. Последний метод более удовлетворителен, так как в этом методе луч света может идти вдоль оси волокна. Однако трудно получить довольно тонкие поперечные срезы. [57]
После изготовления ножа необходимо снабдить его ванночкой, куда попадают получаемые на микротоме срезы. [58]
Однако глобулярные сферолиты, если их не разрезать на тонкие доли с помощью микротома, менее удобны для морфологического изучения, чем сферолиты, выросшие в тонких пленках. В результате двумерные сферолиты изучены более широко, и в большинстве случаев их можно считать эквивалентными поперечным сечениям глобулярных сферолитов. Ниже будет показано, что некоторые различия между теми и другими существуют, но они незначительны и не влияют на многие результаты морфологических исследований, проведенных на тонких пленках. Для наиболее эффективного использования существующих экспериментальных методов желательно работать стойкими пленками полимера, в которых сферолиты достаточно велики и имеют хорошо координированные структуры. Вообще говоря, чем меньше плотность первичных зародышей, тем больше по размерам и лучше сформированы образующиеся из них сферолиты. Скорость гомогенного зародышеобразования можно регулировать выбором соответствующей температуры кристаллизации, однако часто это имеет меньшее значение, чем уменьшение случайного гетерогенного зародышеобразования, связанного с наличием примесей. [59]
 |
Процессы миграции ингредиентов в двухслойном покрытии. [60] |
Страницы: 1 2 3 4 5