Баннет
Cтраница 2
Парафиновый воск оказался неэффективным при ускоренных испытаниях, потому что он расслаивается, особенно при многократных изгибах испытуемых образцов. Баннет [531] суммировал показатели двух основных типов восков, используемых в резиновой промышленности - парафиновых и микрокристаллических восков. [16]
Обработка арилгалогенидов амидом натрия в избытке кипящего диалкиламина [93] явдяется наиболее простым и удобным вариантом. Так, Баннет и Бротертон [14], используя в качестве основания пиперидин, получили с очень хорошими выходами N-арилпиперидины; амины, обладающие пространственными затруднениями, дают более низкие выходы. То, что вторичные амины не реагируют в заметной степени с амидом натрия, в какой-то мере непонятно. Образование арина при действии амида натрия, за которым следует присоединение диалкиламина, не может быть предложено как однозначное объяснение, так как известны случаи аддитивного замещения при наличии реагента амида натрия пиперидин. Во всех случаях си стема гетерогенная, и могут происходить реакции на поверхности. [17]
Это должно привести к уменьшению эффекта сольватации для переходного комплекса. Тем не менее Баннет и Морат указали, что данные Хоуторна не позволяют ответить на вопрос, является ли взаимодействие в переходном комплексе XXXIX между соседними атомами азота и кислорода, несущими разноименные заряды, просто электростатическим или же оно осуществляется посредством водородной связи. [18]
В замещениях этого типа скорость атаки различными реагентами одной и той же ароматической молекулы соответствует степени их нуклеофилыюсти. К такому заключению пришли Баннет и Цалер [263] после сопоставления данных, собранных из многих источников. [19]
В 1925 г. были опубликована работа, в которой Баннет и Пирс описали предложенный ими метод исследования газовой скважины. [20]
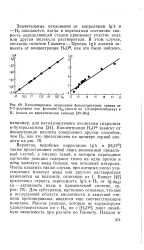 |
Катализируемое основанием фотоотщепление трития от 9 - Т - флуорена как функция Нм ( шкала по 1 3-дифенилиндену и Н - ( шкала по ароматическим аминам [ 39, 39а ]. [21] |
Вероятно, подобные корреляции Igk и [ НзО ] также представляют собой лишь возможный предельный случай, а именно такой, в котором переходное состояние реакции содержит точно на один протон и одну молекулу воды больше, чем исходный материал. Чтобы охватить также случаи, при которых число участвующих молекул воды или другого растворителя изменяется на величину, отличную от 1, Баннет [42] предложил строить зависимость lgk H0 от lgaH2o ( а - активность воды в применяемой системе, ср. Для субстратов, настолько основных, что они в исследуемой области кислотности в заметной степени протонированы, вводятся еще соответствующие поправки. Многие реакции, которые не коррелируют удовлетворительно ни с Н0, ни с [ Н3Ое ], дают линейную зависимость при расчете по Баннету. [22]
Большинство этих предположений может быть подтверждено плюющимися наблюдениями. Выдающееся значение иона диазония как заместителя, ускоряющего пуклеофилыюе замещение галогена, а также питро - или алкоксиль-пой группы в орто - или пара-положениях, хорошо известно; Баннет и Цалер считают этот эффект досадно большим. При диазотировании ароматических аминов указанные группы могут замещаться гидроксилом при взаимодействии с водой или хлором, если при диазотировании употребляется соляная кислота. [23]
Экспериментальные данные скудны и противоречивы. Тронов и Крюгер нашли, что значения отношения фтор / хлор для реакций фенилгалогенидов с пиперидином при 210 С и с метилатом натрия в метаноле при 165 С равны примерно 0 5 16, однако Ли-верис и Миллер оспаривают эти данные и приводят для последней реакции при 202 5 С значение около 10059; Баннет и Бра-зертон 60 также подвергают их сомнению, основываясь на своих опытах с нафтилгалогенидами и пиперидином. Поскольку предполагают, что в этих реакциях происходит атака галогена натриевым комплексом с образованием галогенида натрия, следовало бы ожидать, что отношение фтор / хлор будет значительно меньше единицы. [24]
Поскольку можно считать доказанным каталитическое влияние аминов на реакцию 2 4-динитрохлорбензола с аминами, вполне логично предположить, что и другие основания, например гидроксил - и ацетат-ионы, способны катализировать эту реакцию. Баннет и Пруитт, авторы первой из них [79], утверждают, что реакцию 2 4-динитрохлорбензола и пиперидина в смеси 50 % диоксана и 50 % воды не катализируют ни пиперидин, ни гидроксил-ион. Однако в более поздней работе [74] было достоверно показано, что н-бутиламин катализирует реакцию 2 4-динитрохлорбензола с н-бутилами-ном в той же системе растворителей. Кроме того, результаты этой работы, по-видимому, говорят в пользу предположения о том, что гидроксил-ион также играет роль катализатора. В обоих этих исследованиях трудность заключалась именно в обнаружении каталитического действия иона гид-роксила, так как субстрат реагирует с этим ионом, образуя 2 4-динитрофе-нол, гораздо быстрее, чем с амином, давая N-замещенный анилин. [25]
В 1961 г. Баннет [31] решил обе эти проблемы. Он показал, что шкалы кислотности, применяемые к равновесию в водных растворах кислот, зависят в большой мере от изменения активности растворителя - воды и, следовательно, от количества связанной воды, включая сольватационную, которое высвобождается или связывается с растворенным веществом в результате переноса протона. Высвобождение связанной воды более благоприятствует течению реакций при высокой кислотности, когда раствор менее богат свободными молекулами растворителя - воды. Шкала h0 была построена для выражения равновесия переноса протона от сильно гидрофильных молекул воды к умеренно гидрофильным органическим азотистым основаниям. Шкала h0 прекрасно отражает равновесный перенос протона к умеренно гидрофильным органическим азотистым и органическим кислородным основаниям. Однако, когда высвобождается слишком большое количество связанной воды, что бывает при переносе протона от воды к гидрофобным углеродным основаниям, тогда функция h0 становится неприменимой. Баннет пришел к заключению, с которым следует согласиться, что функция Гаммета / г0 иногда все же дает приближенное описание псевдоравновесного частичного переноса протона и связанного с этим переносом частичного высвобождения воды, протекающих при образовании переходного состояния переноса протона к углероду. [26]
Страницы: 1 2