Митомицин
Cтраница 1
Митомицины - быстродействующие бактерицидные и цитоток-сичные реагенты, и устойчивость к ним клеток некоторых бактерий может быть объяснена только барьерами проницаемости. Интересно, что вирусная ДНК, в отличие от ДНК клеток хозяина, митомицина-ми почти не разрушается. [1]
Митомицин С применяют как противоопухолевый препарат. [2]
Митомицины А, В и С, а также порфиромицин представляют собой комплекс противоопухолевых антибиотиков, продуцируемых несколькими видами Streptomyces. Впервые они обнаружены японскими исследователями в 1956 г., а их строение определено химическим и рентгеноструктурным анализом в 1962 - 1976 гг. Описаны полные синтезы митомицинов и множества их производных и аналогов. Из них ряд соединений проявляет большую активность против отдельных видов опухолей ( лейкопения) и меньшую токсичность. Наиболее поразительной чертой химического строения митомицинов является присутствие в молекулах азиридинового цикла, редко встречающегося среди природных соединений. [3]
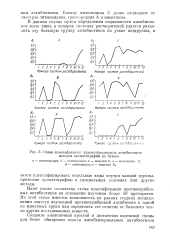 |
Схема классификации красно-фиолетовых антибиотиков методом хроматографии на бумаге. [4] |
Спектр митомицина С резко отличался от спектров литмоцидина, грнзеородина А и мицетинов. [5]
Менисци реакция 43 - Митомицин С 652 Морфин 167 Мочевая кислота 577 Мочевины в синтезе кольц. [6]
Другой антибиотик из Streptomyces, митомицин В ( 82) [ 83а ], представляет собой замещенный толухинон, происхождение которого может иметь много общего с происхождением С7 - звена ансамицинов. [7]
Биологическое действие порфиромицина практически одинаково с действием митомицина. [8]
Этот антибиотик, выделенный из Streptomyces caespifosus является аналогом митомицина С, а именно, N-метилмитомицином С. Токсичность порфироми-цина аналогична токсичности митомицина С, лучше изученного в связи с его применением для лечения рака. [9]
С помощью градиента плотности CS2S04 были изучены ДНК с поперечными сшивками, образующимися в присутствии митомицина [ 69 - - 71, а также ДНК из вируса оспы птиц [72] и В. [10]
С момента открытия в 1956 г. и до сегодняшнего дня много внимания в химической литературе уделяется группе антибиотиков митомицинов и, особенно, митомицинуС 6.413. Объясняется это тем, что пара-хинон 6.413 обладает сильным противоопухолевым действием. Он находит применение в клинике для лечения рака, однако ограниченное. [11]
Образование поперечных связей под действием последних из этих двух факторов происходит между соответствующим образом расположенными тиминовыми или гуаниновыми парами в полимере. Действие антибиотика митомицина С, подавляющего синтез ДНК in vivo, тоже, по-видимому, отчасти определяется тем, что он вызывает сшивание цепей ДНК. В принципе ковалентная связь по типу конец-в-конец, при помощи которой замкнуты в кольцо молекулы кольцевых ДНК, эквивалентна поперечной связи, ибо она также препятствует расплетанию цепей ДНК. Именно поэтому кольцевая двухцепочечная ДНК, например ДНК вируса полиомы, по многим своим свойствам напоминает поперечносшитую ДНК. [12]
Этот антибиотик, выделенный из Streptomyces caespifosus является аналогом митомицина С, а именно, N-метилмитомицином С. Токсичность порфироми-цина аналогична токсичности митомицина С, лучше изученного в связи с его применением для лечения рака. [13]
Спектр поглощения порфиромицина в ультрафиолетовом свете идентичен спектру митомицина С. [14]
Описана перегруппировка некоторых циклопропанов в пирролоиндоли-ны. Так, описан синтез предшественника митозана - биологически активного продукта деградации митомицинов. [15]
Страницы: 1 2