Коллоидная мицелла
Cтраница 2
Кислый раствор должен созревать в течение определенного времени вплоть до появления в нем голубой дымки, свидетельствующей об образовании коллоидной мицеллы, состоящей из большого числа дополнительно заряженных молекул смолы. [16]
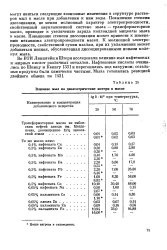 |
Влияние мыл на диэлектрические потери в масле. [17] |
Повышение степени диссоциации, не меняя молионный характер электропроводности, свойственный неувлажненной системе мыла - трансформаторное масло, приводит к увеличению заряда коллоидной мицеллы мыла в масле. Повышение степени диссоциации может привести к изменению механизма электропроводности масел. К молионной электропроводности, свойственной сухим маслам, при их увлажнении может добавиться ионная, обусловленная диссоциированными ионами молекул мыла. [18]
Прежде чем приступить к изложению теории строения коллоидных частиц, необходимо отметить, что термин коллоидная частица носит неопределенный характер: более правильным и более точным является термин коллоидная мицелла. [19]
В работе [64] представления о коллоидной природе битумов были изложены следующим образом: компоненты с хорошо выраженными ароматическими свойствами и наибольшим молекулярным весом наиболее тесно примыкают к ядру коллоидной мицеллы. Вокруг ядра располагаются последовательные слои компонентов со все меньшей ароматичностью и молекулярным весом, переходящие в интерми-це. [20]
 |
Схема перекрытия ионных атмосфер двух сферических частиц. [21] |
Как показали исследования, коллоидные частицы могут беспрепятственно приближаться друг к другу на расстояние Ю - & см. Дальнейшее сближение встречает препятствие со стороны сольватных ( гидратных) оболочек, связанных с ионной атмосферой коллоидной мицеллы. Это и есть расклинивающее давление по Дерягину. Энергия, которая необходима для преодоления этого давления, быстро возрастает и достигает максимума при расстоянии между частицами примерно 10 - 7 - Ю - в см. Ван-дер-ваальсовы силы притяжения между коллоидными частицами непрерывно усиливаются, но их когезионное действие слабее расклинивающего действия тонких сольватных оболочек. В этом случае происходит перераспределение ионов в ионной атмосфере взаимодействующих мицелл, что приводит к появлению дополнительных сил отталкивания. В том случае, когда расстояние между мицеллами становится меньше К) - Ю - йсм, расклинивающее действие быстро уменьшается, достигает нулевого значения и наступает коагуляция. [22]
 |
Схема передвижения коллоидной частицы при электрофорезе ( а и электроосмотического переноса жидкости через капилляр ( б ( С - внутренняя поверхность капилляра. [23] |
В этом случае изменение межфазового потенциала от его максимального значения на поверхности твердой фазы до нулевого целиком происходит в пределах адсорбционного слоя. Такое состояние коллоидной мицеллы называют изоэлектри-ческим состоянием. [24]
 |
Схема передвижения коллоидной частицы при электрофорезе ( а и электроосмотического переноса жидкости через капилляр ( б ( К. - внутренняя поверхность. [25] |
В этом случае изменение межфазового потенциала от его максимального значения на поверхности твердой фазы до нулевого целиком происходит в пределах адсорбционного слоя. Такое состояние коллоидной мицеллы называют изоэлектрическим состоянием. [26]
 |
Схема передвижения коллоидной частицы при электрофорезе ( а и электроосмотического переноса жидкости через капилляр ( б ( К. - внутренняя поверхность капилляра. [27] |
В этом случае изменение межфазового потенциала от его максимального значения на поверхности твердой фазы до нулевого целиком происходит в пределах адсорбционного слоя. Такое состояние коллоидной мицеллы называют изоэлектри-ческим состоянием. [28]
В электрическом поле коллоидная мицелла подвергается изменению, так как частица должна двигаться в одном направлении, а противоионы - в другом. Этот своеобразный электролиз в коллоидных растворах, отделяющий заряженные частицы от проти-воионов мицелл, называется электрофорезом. Исследование электрофореза значительно расширило наши представления о строении коллоидных растворов. [29]
В электрическом поле коллоидная мицелла подвергается изменению, так как частица должна двигаться в одном направлении, а противо-ионы в другом. Этот своеобразный электролиз в коллоидных растворах, отделяющий заряженные частицы от противоионов мицелл, называется электрсфорезом. Исследование электрофореза значительно расширило наши представления о строении коллоидных растворов. [30]
Страницы: 1 2 3 4