Металлический барий
Cтраница 1
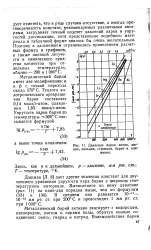 |
Давление паров лития, магния, кальция, стронция, бария и алюминия. [1] |
Металлический барий имеет две модификации: а и р с точкой перехода около 370 С. Теплота аллотропического превращения бария составляет 0 14 ккал / г-атом, плавления 1 83 ккал / г-атом. [2]
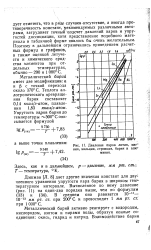 |
Давление паров лития, магния, кальция, стронция, бария и алюминия. [3] |
Металлический барий активно реагирует с водородом кислородом, азотом и парами воды, образуя ионные соединения; окись, гидрид и нитрид. [4]
Металлический барий легко реагирует с водой и многими кислотами. [5]
Металлический барий получают металлотермическим восстановлением окиси или хлорида бария, термическим разложением гидрида и нитрида бария или Ba ( NH3) 6, электролизом расплавленного хлорида бария ( смесей ВаС12 и NaCl, ВаС12 и BaF2) или насыщенного раствора ВаС12 - 2Ы20 на ртутном катоде. Во избежание контактов с воздухом все эти процессы ведут в вакууме или защитной атмосфере. [6]
Металлический барий применяется для металлотермического восстановления америция и кюрия, в антифрикционных сплавах на основе свинца, а также в вакуумной технике. Сплавы свинец - барий вытесняют полиграфические сплавы свинец - сурьма. [7]
Металлический барий легко реагирует с водой и многими кислотами. Гидрид бария - твердое соединение серого цвета, которое легко разлагается водой и кислотами. С углеродом и азотом барий взаимодействует, образуя цианид бария - термически очень устойчивое соединение. [8]
Металлический барий может быть получен путем электролиза расплавленного хлорида бария или электролизом водного раствора хлорида с применением ртутного катода; образующаяся амальгама разлагается при нагревании в атмосфере водорода. [9]
Металлический барий находит лишь ограниченное применение, он взрывоопасен. Растворимые соединения бария ( хлорид, нитрат, гидроксид) высоко токсичны, ингаляция нерастворимых соединений ( сульфат) может приводить к развитию пневмокониоза. Многие из соединений, включая сульфид, оксид и карбонат, могут вызывать локальные раздражения глаз, носовой полости, горла и кожи. Определенные соединения, особенно пероксид, нитрат и хлорат, пожароопасны при использовании и хранении. [10]
 |
Природный кристалл арагонита ( одна из форм карбоната кальция СаС03. [11] |
Металлический барий не находит сколько-нибудь значительного применения. Основными соединениями этого элемента являются сульфат бария BaS04, очень плохо растворимый в воде и разбавленных кислотах, и хлорид бария ВаС12 - 2Н20, растворимый в воде. Сульфат бария встречается в природе в виде минерала барита. [12]
Металлический барий в слитках без металлической оболочки завертывают в 3 - 4 слоя маслонепроницаемой бумаги, помещают в металлическую банку, завальцовывают ее и помещают в металлический контейнер. [13]
Металлический барий не находит широкого применения. Важнейшими соединениями этого элемента являются сульфат бария BaSC4, очень плохо растворимый в воде и в разбавленных кислотах, и хлорид бария ВаС12 - 2Н2О, растворимый в воде. Сульфат бария встречается в природе в виде минерала барита. [14]
Сырой металлический барий очищают перегонкой в вакууме ( 1 - 1 5 мм рт. ст., температура 800) в аппаратуре, подобной применяемой для очистки магния. [15]
Страницы: 1 2 3 4