Металлический барий
Cтраница 3
Металлический плутоний впервые получен восстановлением PuF4 металлическим барием в ториевом тигле при 1400 С. Могут быть применены также другие стандартные методы. [31]
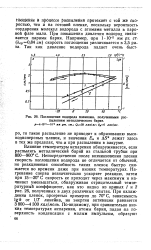 |
Поглощение водорода пленками, полученными распылением металлического бария. [32] |
Влияние температуры испарения обнаруживается, если распылять металлический барий из стальной трубки при 800 - 900 С. Непосредственно после возникновения пленки скорость поглощения водорода не отличается от обычной, но реакциовная способность таких пленок быстро снижается во времени даже при низких температурах. Нагревание сперва незначительно ускоряет реакцию, затем при 15 - 20 С скорость ее проходит через максимум и начинает уменьшаться, обнаруживая отрицательный температурный коэффициент, как это видно из кривых 1 и 2 рис. 26, полученных в двух различных опытах. При охлаждении пленок, прогретых примерно до 70 С, зависимость Igk от 1 / Т линейна, но энергия активации равняется 3 800 - 4 300 кал / моль. [33]
Этим путем может быть обеспечен рост ядер металлического бария. Однако термическое разложение азида бария не обязательно протекает по этому механизму, так как он зависит от специфики в распределении атомов бария. [34]
В металлургии хлорид бария применяют для получения металлического бария электролизом расплава или дистилляцией приготовленной из ВаС12 амальгамы бария. [35]
Металлический протактиний был получен восстановлением тет-рафторида протактиния металлическим барием при температуре 1400 С. Получение металлического протактиния, о котором сообщали в 1934 г. Гроссе и Агрусс [35], было выполнено несколько необычным способом. Окись протактиния в высоком вакууме бомбардировали электронами с энергией 35 кэв или, в другом случав, пентахлорид протактиния термически разлагали на нити накала. [36]
В процессе магнийтермического восстановления окиси бария в вакууме получается металлический барий. [37]
В екш и некий, Иванов А. А., Способ получения металлического бария. [38]
Фосфид бария, Ва3Р2, получают нагреванием в вакууме металлического бария с красным фосфором, а также восстановлением фосфатов бария углем в электрической печи. [39]
Он легко может быть восстановлен222 в металлический с помощью металлического бария при 1100 С. [40]
В результате восстановительного активирования в оксидном слое образуется запас металлического бария. [41]
 |
Устройство катодов. бариево-вольфрамового ( а, оксидного ( б, прессованного ( в. [42] |
Главную роль в эмиссии оксидного катода играют окись бария и металлический барий. Окись бария является ионным кристаллом, в котором отсутствуют электроны проводимости. [43]
К суспензии 8 3 г ( 0 06 г-атома) мелко измельченного металлического бария в 5 мл бензола в трехгорлой колбе добавлено в атмосфере азота 22 2 г ( 0 18 моля) диэтилцинка. При перемешивании смесь медленно нагрета до 65 - 70 С. После охлаждения до комнатной температуры добавлено 75 - 100 мл абсолютного эфира, и кипячение продолжено 1 - 1 5 часа. Отстоявшаяся суспензия отфильтрована через асбестовую ткань; полученный раствор проанализирован двумя способами: а) 2 мл раствора гидролизованы до гидроокиси бария с последующим титрованием серной кислотой; б) из аликвотной части барий в виде сульфата определен гравиметрически. [44]
При нагревании в атмосфере воздуха з интервале температур 260 - 600 металлический барий соединяется с азотом и дает нитрид Ba3N2, плавящийся при - 1000 и мало летучий. Соединение это при нормальной температуре достаточно прочно, так как образуется с выделением 89 9 ккал / моль, но начиная с 300 оно реагирует с водородом, а ори красном калении вступает во взаимодействие с окисью углерода. [45]
Страницы: 1 2 3 4