Баррер
Cтраница 3
Баррер [10] рассчитал теплоту адсорбции азота, аргона и водорода на графите и нашел, что над центром шестиугольника из атомов углерода она больше, чем над одной из вершин, приблизительно на 400 кал для азота и аргона и приблизительно на 180кал для водорода. Если тепловая энергия RT мало отличается от этих энергий активации, то молекулы должны свободно перемещаться по поверхности. Отсюда Баррер делает вывод, что водород может свободно перемещаться по поверхности при 90 К, а азот и аргон - при 200 К. [31]
 |
Зависимость сорб. [32] |
Баррер и Денни [40] провели синтез монтмориллоноидов в присутствии избытка основания ( гидроокиси метиламмония), что являлось отличительной чертой указанного синтеза. [33]
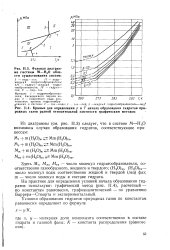 |
Фазовая диаграмма системы М - Н20 области существования систем.| Кривые для определения р и Т начала образования гидратов природных газов разной относительной плотности графическим методом. [34] |
Баррера - Стюарта и экспериментальный. [35]
Баррера [19]) измерил скорость потока различных газов через пористые пластинки и нашел, что скорость потока является функцией от среднего давления внутри пластинки. Предположив, что пористая структура представляет собой сочетание пор, где некоторые из них располагаются последовательно, а некоторые параллельно, Адзуми показал, как уравнение ( 14в) можно использовать для расчета среднего радиуса поры из измерении скорости потока. [36]
Баррером [64] для водорода, аргона и азота на графите в области температуры 71 - 288 К. Кривые 2 представляют изменение qd при адсорбции первых нескольких десятых см3 газа. Максимальное значение теплоты адсорбции в кривых Баррера отвечает покрытию адсорбированным веществом очень малой части поверхности. Так как среднее расстояние между адсорбированными молекулами слишком велико, чтобы привести к заметному взаимодействию, то причину максимума следует искать в структуре адсорбента. Одна из возможностей заключается в том, что различные плотности упаковки атомов углерода в призматических и базисных гранях вызывают изменение теплот адсорбции. В этом случае мы должны ожидать больших величин теплот на призматических поверхностях, так как призматические площади малы, и бэлыние величины qd встречаются только на малой части поверхности. Однако, вычисление показывает, что теоретическая теплота адсорбции на призматических гранях меньше, чем на базисных. Большие начальные величины теплот адсорбции Баррер приписывает адсорбции в трещинах адсорбента. По мере того как угол между двумя поверхностями, которые образуют трещину, становится более острым, она приближается к трещине с параллельными стенками. В такой трещине теплота адсорбции должна быть вдвое больше, чем на плоской поверхности. Начальное и конечное значения qd действительно близки как раз к этому отношению 2: 1, а именно - они составляют 4600 и 2500 кал / моль для азота, 4100 и 2400 для аргона и 2000 и 1100 для водорода. [37]
Баррером [64] для водорода, аргона и азота на графите в области температуры 71 - 288 К. Кривые 2 представляют изменение qd при адсорбции первых нескольких десятых см3 газа. [38]
Недавно Баррер привел ряд хороших примеров изибратель-ного обменного поведения природных цеолитов, обусловленного в первую очередь их структурой. На шабазите также удается обмен Li, Са2, Ва2 и Sr2, в то время как магний обмениваться не может. Это различное поведение Баррер объясняет частично реакциями, протекающими при гидротермальных процессах, частично состоянием каналов решетки. Вследствие основного обмена кубическая решетка анальцима легко превращается в тетрагональную; у шабазита подобного процесса не происходит. [39]
Опытами Баррера были намечены пути синтеза в условиях пониженных температур ( 100 С) при нормальном давлении. [40]
 |
Скорость поглощения вспомогательного газа кристаллической решеткой гидрата хлороформа. [41] |
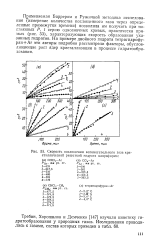
Применяемая Баррером и Ружичкой методика исследования ( измерение количества поглощенного газа через определенные промежутки времени) позволила им получить при постоянных Р, t серию однозначных кривых, практически прямых ( рис. 53), характеризующих скорость образования указанных гидратов. На примере двойного гидрата тетрагидрофу-ран Ar эти авторы подробно рассмотрели факторы, обусловливающие рост ядер кристаллизации в процессе гидратообра-зования. [42]
Как предполагает Баррер [13], восемь тетраэдров могут соединяться, образуя куб; 12 тетраэдров образуют гексагональную призму, а 24 тетраэдра - кубооктаэдр. Внедрение этих крупных групп, например кубооктаэдра, в кристаллическую решетку приводит к образованию структур с весьма большим объемом пор молекулярных размеров; и даже при введении дополнительных ионов металлов остается достаточно пространства для вмещения многих органических молекул. В цитируемой обзорной статье [13] приводится ряд примеров подобных широко распространенных структур. Как отмечается в многочисленных работах Баррера и других [22], можно получать структуры, размер пор которых изменяется в широких пределах. Эти возможности изменения основных характеристик цеолитов достигаются варьированием как структуры скелета, так и ионов металлов. [43]
 |
Коэффициенты водородопроницаемости, диффузии и сорбции водорода при 20 С. [44] |
Дейнеса - Баррера, который применяется для определения D ( см. стр. [45]
Страницы: 1 2 3 4