Барьер - потенциальная энергия
Cтраница 2
Теория туннельного переноса электрона, разработанная Вайсом [13], Маркусом, Цволинским и Эйрингом [14], позволяет понять процессы переноса электрона. Возможность прохождения электронов через барьер потенциальной энергии, что невозможно с точки зрения классической механики - хорошо известное явление в квантовой механике. В результате туннельного эффекта перенос электрона может происходить на расстояниях значительно больших, чем те, которые соответствовали бы фактическому столкновению реагирующих веществ. Таким образом, туннельный эффект связан с пространственной экспансией электронных орбиталей, упомянутой в связи с процессами переноса в газовой фазе. [16]
Почему атомы радия не испускают сразу же весь содержащийся в них гелий. Это объясняется тем, что существует барьер потенциальной энергии, который противодействует выходу содержащихся в ядре заряженных частиц. Частица, несущая два положительных электрических заряда, имеет некоторую вероятность проникнуть сквозь этот барьер благодаря своей кинетической энергии, соответствующей разности масс между суммой масс атомов радона и гелия и массой атома радия. [17]
Чтобы вызвать превращение в случае экзоэнергетической реакции, достаточно, чтобы падающая частица была захвачена, какова бы ни была ее кинетическая энергия. Выход превращения определяется вероятностью проникновения падающей частицы через барьер потенциальной энергии. В случае эндоэнергстической реакции, когда сумма масс реагирующих ядер меньше суммы масс образовавшихся ядер, превращение возможно лишь при условии, что падающая частица обладает некоторой минимальной энергией, независимо от вероятности проникновения через барьер потенциальной энергии. В экзоэпергетических реакциях кинетическая энергия выброшенной частицы может быть больше кинетической энергии падающей частицы. [18]
Наши выводы состоят в том, что правила работают в смысле предсказания существующих энергетических барьеров. В случае правил отбора по спину это ограничение представляет собой одну из возможностей-другими являются барьеры потенциальной энергии. Главный недостаток в том, что величины барьеров оценить нелегко. Они лежат в диапазоне от 100 до 10 ккал / мол ь или даже меньше. В подавляющем большинстве случаев реакции, которые, согласно предсказаниям, запрещены, по-видимому, не протекают. Это приводит к мысли, что энергетические барьеры достаточно значительны. [19]
 |
Конструкция и схема диода. [20] |
Когда же катод накален при помощи извне подведенной энергии до высокой температуры, часть электронов приобретает достаточную энергию для преодоления барьера потенциальной энергии: эти электроны излучаются с поверхности катода в окружающее внутреннее пространство электронной лампы, имеющее высокую степень разрежения. В этом случае вылет электрона с поверхности металла становится возможным, когда кинетическая энергия электрона внутри металла становится больше величины барьера потенциальной энергии. [21]
Большинство графиков в аррениусовских координатах линейно в пределах экспериментальной ошибки даже в расширенном интервале температур, и до сих пор мы предполагали, что ЕА не меняется с температурой. Если это действительно так, то ЕА можно отождествить с ее значением при 0 К, и она является мерой высоты барьера потенциальной энергии без учета тепловой энергии. Однако известно, что для некоторых реакций переноса протона график нелинеен из-за квантовомеханического туннельного эффекта и что даже если искривление не заметно в умеренном температурном интервале, высота энергетического барьера может быть на 20 % больше значения ЕА ( стр. Это довольно специальный случай, но в связи с ним возникает общий вопрос о линейности графиков в аррениусовских координатах и о связи ЕА с высотой барьера [ 7 ( стр. [22]
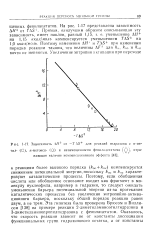 |
Зависимость Д / / от - Г AS для реакций гидразина с п-ме. [23] |
ОК характеризуют каталитические процессы. Поэтому, если обобщенная кислота или обобщенное основание входит как фрагмент в молекулу нуклеофила, например в гидразин, то следует ожидать уменьшения барьера потенциальной энергии из-за протекания каталитических процессов без увеличения энтропийно-актива-ционного барьера, поскольку общий порядок реакции равен двум, а не трем. Эта гипотеза была проверена Брюсом и Виллисом [138] на примере реакции 2-диметиламиноэтилгидразина и 3-диметиламииопропилгидразина с фенилацетатом. [24]
Выводы предыдущего раздела таковы, что природа отдает предпочтение механизмам, состоящим из последовательности мономолекулярных и бимолекулярных реакций. Отбор этих стадий происходит на вероятностной или энтропийной основе как более выгодных по сравнению с высокосогласованными процессами, в которых три или более молекул должны действовать согласованно, чтобы дать благоприятный барьер потенциальной энергии. Трудность участия нескольких молекул в одном столкновении подчеркивается изучением сложности столкновений даже двух молекул. [25]
Если потенциальная функция молекулы VN имеет п симметрически-эквивалентных минимумов без заметного проникновения локализованных волновых функций ( туннелирования) через барьеры между этими минимумами, то каждый уровень будет иметь n - кратное конфигурационное вырождение. Если имеется туннелирование сквозь барьеры, вырождение снимается, а это случается, когда высота барьера невелика по сравнению с колебательной энергией. В действительности всегда имеет место некоторое туннелирование, так как барьеры потенциальной энергии не являются бесконечно высокими, однако разрешение, достигаемое в эксперименте, часто не является достаточно высоким, чтобы заметить такое расщепление. Это имеет место и в случае метана. [26]
Ясно, что для этих реакций ДА может включать заметное количество тепловой энергии, кроме потенциальной энергии, которая измеряется значением ДА при 0 К. Кроме того, это может оказаться верным для реакций, дающих графики Арре-ниуса, кажущиеся линейными, так как значение Дд / с должно-по крайней мере равняться ( - 10 кал-моль 1-град 1), прежде чем появятся отклонения, которые можно заметить в обычных кинетических экспериментах, а это могло бы привести к разности до 3 ккал-молъ 1 между ДА и потенциальной энергией. Наблюдаемые для таких реакций значения ДА нельзя, следовательно, просто отождествить с высотой барьера потенциальной энергии. Однако это будет оправдано в качестве первого приближения для реакций, происходящих без изменения заряда иона, и особенно для сравнения ряда близких реакций при одной и той же температуре, как на стр. [27]
Чтобы вызвать превращение в случае экзоэнергетической реакции, достаточно, чтобы падающая частица была захвачена, какова бы ни была ее кинетическая энергия. Выход превращения определяется вероятностью проникновения падающей частицы через барьер потенциальной энергии. В случае эндоэнергстической реакции, когда сумма масс реагирующих ядер меньше суммы масс образовавшихся ядер, превращение возможно лишь при условии, что падающая частица обладает некоторой минимальной энергией, независимо от вероятности проникновения через барьер потенциальной энергии. В экзоэпергетических реакциях кинетическая энергия выброшенной частицы может быть больше кинетической энергии падающей частицы. [28]
Многие из многоатомных молекул являются нелинейными и жесткими. Оставшаяся часть настоящей главы посвящена таким молекулам; линейные и нежесткие молекулы рассмотрены в гл. Под термином жесткая молекула в настоящей книге подразумевается молекула, находящаяся в электронном состоянии с единственной равновесной конфигурацией ядер или же в состоянии, в котором барьеры, разделяющие различные равновесные конфигурации на поверхности потенциальной энергии, непреодолимы. Для нежестких молекул ( типа аммиака) барьеры потенциальной энергии преодолимы, а туннелирование молекулы между потенциальными минимумами приводит к расщеплениям и сдвигам колебательно-вращательных уровней энергии, наблюдаемым в спектрах. [29]
В этой главе показано, что ни одно из этих допущений не является вполне точным. Значение Е & реакции в принципе зависит от температуры и для некоторых реакций такое изменение можно заметить при тщательных измерениях. Вследствие этого нельзя точно отождествлять Е с высотой барьера потенциальной энергии, несмотря на то что, по-видимому, не возникает большой ошибки, если относительные значения для данного ряда реакций при данной температуре интерпретировать как изменения потенциальной энергии. Наконец, растяжение химических связей в реагирующих молекулах является только одним из факторов, дающих вклад в ЕА, к которым относятся также отталкивание, десольватация, ион-дипольные взаимодействия и диффузия. В случае быстрых реакций может преобладать один из них; выше было приведено много примеров, когда стадией, лимитирующей скорость, является диффузия, а также несколько примеров, где скорость лимитируется десольватацией. Исследование быстрых реакций, несомненно, позволит оценить значение этих и аналогичных энергетических факторов, которые могут давать только малый вклад в энергии активации реакций, исследуемых обычными кинетическими методами, но становятся важными, когда Е & относительно мала. [30]
Страницы: 1 2 3