Энергетический барьер
Cтраница 4
Аналогично энергетический барьер для вращения из заторможенной формы в заслоненную составляет только 2 - 3 ккал / моль, однако переход симметрии А1и в нормальном этане должен соответствовать очень большому энергетическому промежутку. Вращения вокруг простых связей теорией эффекта Яна-Теллера второго порядка корректно не предсказываются. [46]
Энергетический барьер Еа определяется как предел, который должна преодолеть молекула внутри эластомера ( за счет дополнительной кинетической или тепловой энергии) для совершения - перескока в новое положение. Если к эластомеру не приложена тангенциальная сила, то поверхностные молекулы совершают перескоки в зоне контакта с равной вероятностью во всех направлениях. При приложении тангенциальной силы перескоки происходят преимущественно в направлении действия силы. [47]
Начальный энергетический барьер U0, как показывает табл. 11, меняется от материала к материалу и при этом оказывается близким к величине энергии активации распада межатомных связей в твердых телах: в металлах-к энергии сублимации, а в полимерах - к энергии активации процесса термодеструкции. С другой стороны, Uo для данного материала, как оказалось, не зависит от всевозможных структурных изменений. Иначе говоря, как коэффициент т0, так и U0 оказываются нечувствительными к изменениям структуры величинами. [48]
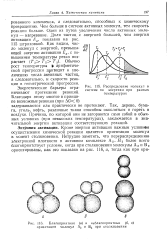 |
Благоприятная ( а и неблагоприятные ( б, в ориентации молекул А2 и В2 при столкновении. [49] |
Энергетические барьеры огра - Рис - 115 - Распределение молекул в ничивают протекание реакций. [50]
Нулевой энергетический барьер U0, согласно работам Журкова с сотрудниками [70, 79-82], примерно равен энергии химической связи в полимерах. Все эти факторы сильнее сказываются на величине у - структурно-чувствительном коэффициенте. [51]
Экспериментальный энергетический барьер, называемый энергией активациии, представляет собой разность потенциальных энергий начального и переходного состояний. Однако ни способ приближения атома X к молекуле YZ, ни путь атома Z, когда он покидает вновь образовавшуюся молекулу XY, не были конкретизированы. Атом X может приближаться под прямыми углами к связи Y - Z в направлении ее центра или в направлении атома Y или он может приближаться к Y вдоль оси связи Y-Z. Теоретически можно рассчитать в рамках приближения Борпа - Оппенгенмера энергию трехэлектронной системы для любых относительных положений X, Y n Z, предполагая, что ядра неподвижны. Если это сделать для любых возможных расположений X, Y и Z, то получим поверхность потенциальной энергии, имеющую области низкой потенциальной энергии, когда X находится на большом расстоянии, a Y-Z имеет нормальную длину связи, а также тогда, когда Z находится на большом расстоянии, а X-Y имеет нормальную длину связи. Между этими областями низкой потенциальной энергии будет существовать барьер, когда X, Y и Z находятся на близких расстояниях друг от друга. Нэп-низшая точка на барьере между областью, описывающей X и YZ, и областью XY и Z есть переходное состояние, а конфигурация трех ядер в этой точке представляет собой активированный комплекс. [52]
Экспериментальный энергетический барьер, называемый энергией активацшш, представляет собой разность потенциальных энергий начального и переходного состояний. Однако ни способ приближения атома X к молекуле YZ, ни путь атома Z, когда он покидает вновь образовавшуюся молекулу XY, не были конкретизированы. Атом X может приближаться под прямыми углами к связи Y - Z в направлении ее центра или з направлении атома Y или он может приближаться к Y вдоль оси связи Y - Z. Теоретически можно рассчитать в рамках приближения Борна - Оппенгеймера энергию трехэлектронной системы для любых относительных положений X, Y и Z, предполагая, что ядра неподвижны. Если это сделать для любых возможных расположений X, Y и Z, то получим поверхность потенциальной энергии, имеющую области низкой потенциальной энергии, когда X находится на большом расстоянии, a Y - Z имеет нормальную длину связи, а также тогда, когда Z находится на большом расстоянии, а X - Y имеет нормальную длину связи. Между этими областями низкой потенциальной энергии будет существовать барьер, когда X, Y и Z находятся на близких расстояниях друг от друга. Наинизшая точка на барьере между областью, описывающей X и YZ, и областью XY и Z есть переходное состояние, а конфигурация трех ядер в этой точке представляет собой активированный комплекс. [53]
Энергетический барьер AU между указанными двумя положениями равновесия относительно мал. С увеличением равномерно распределенного напряжения в плоскости скольжения от внешних сил на величину Ат дислокация смещается на расстояние Ах; при этом расстояние между обеими дислокациями увеличивается или уменьшается, однако центр диполя остается в исходном положении. [54]
 |
Благоприятная ( а и неблагоприятные ( б, а ориентации молекул А2 и В2 при столкновении. [55] |
Энергетические барьеры огра - Рис - 115 Распределение молекул в ничивают протекание реакций. [56]
Энергетический барьер экзотермической химической реакции обусловлен перестройкой электронной структуры реагирующих частиц. Если атом А реагирует с молекулой ВС, то в реакции рвется связь В-С и образуется связь А - В. Такую перестройку приближенно можно описать как суперпозицию двух волновых функций: г з аг А, вс сг) АВ, с, где т) А, вс описывает взаимодействие А с молекулой ВС, а вторая - атома С с молекулой АВ; коэффициенты а и с меняются вдоль координаты реакции. [57]
Энергетический барьер экзотермической химической реакции обусловлен перестройкой электронной структуры реагирующих частиц. Если атом А реагирует с молекулой ВС, то в реакции рвется связь В - - С и образуется связь А - В. Такую перестройку приближенно можно описать как суперпозицию двух волновых функций: г з - - а я) д, Вс сгрдв, с, где д, вс описывает взаимодействие А с молекулой ВС, а фдв, с - атома С с молекулой АВ; коэффициенты а и с меняются вдоль координаты реакции. Качественное представление об общем характере поверхности потенциальной энергии дает рассмотрение двух независимых поверхностей, одна из которых описывается функцией фА, вс, другаяг здв, с - Эти две поверхности пересекаются. При взаимодействии А с ВС пересечение исчезает и образуются нижняя и верхняя поверхности потенциальной энергии, система движется по нижней поверхности. [58]
Энергетический барьер U пристраивания молекул к поверхности, зародыша имеет важное значение при затвердевании силикатных расплавов и органических жидкостей, особенно высокомолекулярных веществ. Величина U соответствует в этом случае по своему смыслу энергии активации диффузии молекулы или ее отдельных сегментов из объема жидкой фазы к поверхности зародыша. При быстром охлаждении таких жидкостей до температур, значительно меньших температуры Тпл-AT, скорость образования кристаллических зародышей оказывается очень малой, а вязкость очень большой и жидкость переходит в аморфное стеклообразное состояние. [59]
 |
Зависимость частоты возникновения / зародышей новой фазы от переохлаждения А Г. [60] |
Страницы: 1 2 3 4 5