Энергетический барьер - активация
Cтраница 2
Для того чтобы реагенты могли вступать во взаимодействие и образовывать продукты, они должны обладать определенным минимумом энергии, который называется энергией активации. При значительной энергии активации ли1иь очень небольшая часть всех столкновений между реагентами обеспечивает их энергией, необходимой для преодоления энергетического барьера активации и образования продуктов реакции. [16]
На рис. 13.5 показаны кривые распределения молекул по кинетической энергии при двух различных температурах. Ясно видно, что при более высокой температуре Т2 большая часть молекул имеет энергию, превосходящую условно выбранную энергию Е, которую можно назвать энергетическим барьером активации. Таким образом, в зависимости от того, каков в действительности энергетический барьер активации конкретной химической реакции, при повышении температуры должно произойти то или иное возрастание скорости реакции, поскольку при этом увеличивается доля молекул реагентов, способных вступать в реакцию. [17]
В ферментативном катализе не происходит ничего такого, чего не могло бы произойти без помощи катализатора. Молекула воды вполне способна приблизиться к цепи белка, как показано в уравнении ( 21 - 1), и расщепить ее на части, отдав группу - ОН левой половине цепи и группу - Н правой половине цепи. Однако энергетический барьер активации этой прямой реакции чрезвычайно высок, и поэтому такая реакция должна быть крайне медленной. [18]
На рис. 13.5 показаны кривые распределения молекул по кинетической энергии при двух различных температурах. Ясно видно, что при более высокой температуре Т2 большая часть молекул имеет энергию, превосходящую условно выбранную энергию Е, которую можно назвать энергетическим барьером активации. Таким образом, в зависимости от того, каков в действительности энергетический барьер активации конкретной химической реакции, при повышении температуры должно произойти то или иное возрастание скорости реакции, поскольку при этом увеличивается доля молекул реагентов, способных вступать в реакцию. [19]
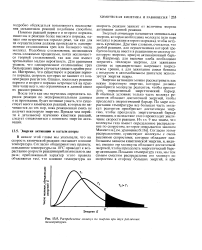 |
Распределение молекул по энергии при двух различных температурах. [20] |
Энергию активации можно рассматривать как некую пороговую энергию, которую должны приобрести молекулы реагентов, чтобы преодолеть определенный энергетический барьер. В обычных условиях только часть молекул реагентов обладает достаточной энергией, чтобы преодолеть энергетический барьер. По мере возрастания температуры все большая часть молекул реагентов приобретает достаточную энергию, чтобы преодолеть энергетический барьер активации, и вследствие этого происходит увеличение скорости реакции. Согласно этому распределению, существуют молекулы с очень высокими скоростями, которые обладают наибольшим запасом кинетической энергии, и, видимо, именно эти молекулы обладают достаточной энергией, чтобы преодолеть энергетический барьер активации. [21]
Энергию активации можно рассматривать как некую пороговую энергию, которую должны приобрести молекулы реагентов, чтобы преодолеть определенный энергетический барьер. В обычных условиях только часть молекул реагентов обладает достаточной энергией, чтобы преодолеть энергетический барьер. По мере возрастания температуры все большая часть молекул реагентов приобретает достаточную энергию, чтобы преодолеть энергетический барьер активации, и вследствие этого происходит увеличение скорости реакции. Согласно этому распределению, существуют молекулы с очень высокими скоростями, которые обладают наибольшим запасом кинетической энергии, и, видимо, именно эти молекулы обладают достаточной энергией, чтобы преодолеть энергетический барьер активации. [22]
Совместное действие всех перечисленных факторов и определяет отличия промышленной химии от академической науки. Конечно, в обоих случаях действуют химические принципы и законы термодинамики. Одинаково и определение катализатора как вещества, которое изменяет скорость реакции и при этом не расходуется. Катализаторы не влияют на положение равновесия и не могут обеспечить протекание реакции, запрещенной термодинамикой. При действии катализатора снижается энергетический барьер активации реакций, идущих с уменьшением свободной энергии. В соответствии с законами термодинамики и химии катализаторы обеспечивают энергетически менее затрудненные пути реакции, но это позволяет эффективнее ис пользовать сырье в перерабатывающей и химической промышленности. [23]
Страницы: 1 2