Моногидрат - хлорная кислота
Cтраница 1
Моногидрат хлорной кислоты НС1О4 Н2О представляет собой негорючее кристаллическое вещество, содержащее 84 8 % масс, хлорной кислоты. При соприкосновении с расплавленным моногидратом бумага, древесина и другие легкогорючие материалы самовоспламеняются. Обычная товарная хлорная кислота имеет концентрацию 70 - 72 % и является самой сильной из кислот. На холоде 72 % - ная кислота взаимодействует с активными металлами, при этом выделяется водород и образуются перхлораты, которые в чистом виде являются взрывчатыми веществами. [1]
Моногидрат хлорной кислоты НСЮ4 - Н2О представляет собой негорючее кристаллическое вещество, содержащее 84 8 % ( масс.) хлорной кислоты. При соприкосновении с расплавленным моногидратом бумага, древесина и другие легкогорючие материалы самовоспламеняются. Обычная товарная хлорная кислота имеет концентрацию 70 - 72 % и является самой сильной из кислот. На холоде 72 % - ная кислота взаимодействует с активными металлами, при этом выделяется водород и образуются перхлораты, которые в чистом виде являются взрывчатыми веществами. [2]
Моногидрат хлорной кислоты НС1О4 - Н2О, представляет собой негорючее кристаллическое вещество, содержащее 84 8 % вес. [3]
Моногидрат хлорной кислоты НС1О4 - Н20, представляет собой негорючее кристаллическое вещество, содержащее 84 8 % вес. [4]
Необычные свойства моногидрата хлорной кислоты, в особенности высокая температура плавления ( 49 9 С), давно наводили на мысль о его особой структуре. Предполагалось, что ион оксония НзО, существование которого в водных растворах постулировалось для объяснения аномальной подвижности протона в воде, является реальным элементом кристаллической структуры моногидрата. [5]
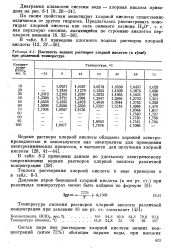 |
Плотность водных растворов хлорной кислоты ( в при различной температуре. [6] |
По своим свойствам моногидрат хлорной кислоты существенно отличается от других гидратов. [7]
Вода в виде моногидрата хлорной кислоты гндратирует ион железа. [8]
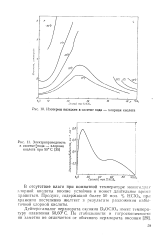 |
Изотермы вязкости в системе вода - хлорная кислота. [9] |
В отсутствие влаги при комнатной температуре моногидрат хлорной кислоты вполне устойчив и может длительное время храниться. Продукт, содержащий более 50 мол. [10]
 |
Диаграммы плавкости системы С1207 - S03 - Н20 ( а и разреза Н2804 - НС104 ( б. [11] |
Общий строй диаграммы подтверждает большую устойчивость моногидрата хлорной кислоты по сравнению с другими кристаллизующимися в данной системе соединениями. Достаточно отчетливо выраженные поля со складками несингулярного типа отвечают первичной кристаллизации серной кислоты и ее моногидрата. [12]
Стандартные теплоты образования изоморфных кристаллов перхлората аммония и моногидрата хлорной кислоты Н3О С1О7 составляют - 69 и - 92 ккал / моль соответственно. Приняв, что энергии решеток обоих соединений одинаковы, определите сродство воды к протону. [13]
При этом выделяется смесь кристаллов перхлората нитрония и моногидрата хлорной кислоты. Перхлорат нитрония отделяют дробной кристаллизацией из его растворов в безводной азотной кислоте или в нитрометане. Остатки маточного раствора после фильтрования могут быть удалены отгонкой нитрометана или хлорной и азотной кислот при нагревании в вакууме. [14]
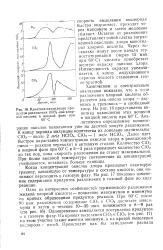 |
Кинетика накопления продуктов разложения 100 % - ной хлорной кислоты в жидкой фазе при 60 С. [15] |
Страницы: 1 2