Монооксид - азот
Cтраница 1
Монооксид азота выполняет в организме роль нейромедиато-ра, развивает иммунные реакции и участвует в системе долговременной памяти. За это открытие ученым была, присуждена Нобелевская премия в области медицины за 1998 г. В настоящее время ведутся интенсивные работы по синтезу и поиску новейших лекарственных веществ, генерирующих NO в организме. [1]
Монооксид азота поступает в атмосферу в результате процессов сгорания, протекающих в природе, и в виде продукта жизнедеятельности бактерий. Общее количество оксидов азота из природных источников в мировом масштабе оценивается в 450 млн. т / год. [2]
Монооксид азота оказывает вредное действие на гемоглобин крови, который превращается в нитрогемоглобин. Степень воздействия NOx на организм человека приблизительно в 10 раз сильнее воздействия СО. [3]
Монооксид азота применяется для получения азотной кислоты. [4]
Монооксид азота термодинамически неустойчив. [5]
Монооксид азота проявляет и окислительные, и восстановительные свойства. [6]
Монооксид азота может быть лигандом в комплексных соединениях. При составлении названий комплексных соединений, в которых NO выступает в качестве лиганда его называют нитрозил. Например, [ Fe ( H2O) 5NO ] SO4 - сульфат нит-розилпентаакважелеза ( П), [ Fe ( NO) 4 ] - тетранитрозилжелезо, Na2 [ Fe ( NO) ( CN) 5 ] - пентацианонитрозилферрат ( Ш) натрия. [7]
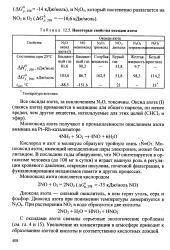 |
Некоторые свойства оксидов азота. [8] |
Монооксид азота, имеющий неподеленные пары электронов, может быть лигандом. В последние годы обнаружено, что NO синтезируется в организме человека ( до 100 мг в сутки) и играет важную роль в регуляции кровяного давления, секреции инсулина, почечной фильтрации, в функционировании механизмов памяти и других процессах. [9]
Монооксид азота NO [ оксид азота ( П), окись азота ] - бесцветный, малорастворимый в воде газ. Он токсичен, связывает гемоглобин крови. [10]
Получают монооксид азота действием азотной кислоты ( разб. [11]
Кипит жидкий монооксид азота при - 151 8 С. [12]
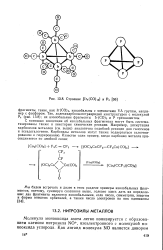 |
Строение [ Ir4 ( CO 12l и Р4. [13] |
Молекула монооксида азота легко ионизируется с образованием катиона нитрозила NO, изоэлектронного с молекулой монооксида углерода. [14]
На образование монооксида азота NO затрачивается большое количество энергии, идущей на разрыв связей в молекулах исходных веществ. Энергия связи в молекуле NO составляет 627 кДж / моль; это значительно меньше, чем в молекуле азота. Поэтому образование NO происходит при очень высокой температуре - выше 1500 С. В промышленности азот получают из воздуха. Для этого воздух сжижают при высоком давлении и низкой температуре, а затем подвергают фракционированной перегонке. [15]
Страницы: 1 2 3 4