Моноприсоединение
Cтраница 1
Моноприсоединение карбэтоксикарбена к 1 3 - и 1 4-диенам происходит легко. [1]
При проведении моноприсоединений к акрилонитрилу или метил-винилкетону реакционную смесь оставляют на ночь, при моноприсоединениях к эфирам акриловой кислоты - на 24 час. При синтезе бис-аддуктов время соответственно удваивают. После этого реакционную смесь перегоняют в вакууме. [2]
Эти реакции моноприсоединения не сопровождаются образованием теломеров. [3]
При проведении моноприсоединений к акрилонитрилу или метил-винилкетону реакционную смесь оставляют на ночь, при моноприсоединениях к эфирам - акриловой кислоты - на 24 час. При синтезе бмс-аддуктов время соответственно удваивают. После этого реакционную смесь перегоняют в вакууме. [4]
Обычно повышенные выходы продуктов моноприсоединения, получающиеся в реакциях с ос р-ненасыщенными эфирами и кетонами, такими, как этиловый эфир малеиновой кислоты и окись мезитила, но не при взаимодействии с простыми олефинами типа октена-1, можно объяснить тем, что ацильный радикал ведет себя как очень сильная нуклеофильная частица. Такое объяснение возможно и верно, однако никакие прямые сравнения поведения ацильных радикалов с другими радикалами автору не известны. Правда, третий из приведенных выше примеров указывает на то, что ацетильный заместитель в некоторых случаях служит лучшим стабилизатором соседнего радикального центра в аддукт-радикале, чем два метильных заместителя. [5]
Стабилизация все еще активных продуктов моноприсоединения происходит в результате дальнейших реакций присоединения или за счет реакций конденсации. Если метанол или этанол прибавляют в мягких условиях, то образуются преимущественно геми-нальные диалкоксииминоизоиндоленины XXXII, которые относительно устойчивы. Не менее стойким оказывается и продукт присоединения к фталонитрилу 1 моль этиленгликоля. [6]
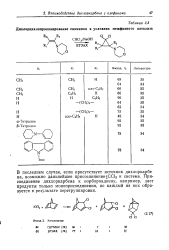 |
Дихлорциклопропанироваиие енаминов в условиях межфазного катализа. [7] |
Присоединение дихлоркарбена к норборнадиену, например, дает продукты только моноприсоединения, но каждый из них образуется в результате перегруппировки. [8]
При проведении моноприсоединений к акрилонитрилу или метил-винилкетону реакционную смесь оставляют на ночь, при моноприсоединениях к эфирам - акриловой кислоты - на 24 час. При синтезе бмс-аддуктов время соответственно удваивают. После этого реакционную смесь перегоняют в вакууме. [9]
При проведении моноприсоединений к акрилонитрилу или метил-винилкетону реакционную смесь оставляют на ночь, при моноприсоединениях к эфирам акриловой кислоты - на 24 час. При синтезе бис-аддуктов время соответственно удваивают. После этого реакционную смесь перегоняют в вакууме. [10]
Однако в случае реакций в условиях МФК часто наблюдается присоединение по нескольким связям, и иногда процесс трудно остановить на стадии моноприсоединения. Если имеется несколько изолированных кратных связей, то в первую очередь будет атакована наиболее электронообогащенная. [11]
Взаимодействие дизамещенных ацетиленов с ди-галогенкарбенами в некоторых случаях сопровождается побочной реакцией, заключающейся в том, что вторая молекула дигалоген-карбена как бы внедряется в С-С - связь между циклом и алкильной группой и наряду с основным продуктом моноприсоединения получается хлорид с олефиновой структурой. [12]
Взаимодействие дизамещенных ацетиленов с ди-галогенкарбенами в некоторых случаях сопровождается побочной реакцией, заключающейся в том, что втор ая молекул а дигалоген-карбена как бы внедряется в С-С - связь между циклом и алкильной группой и наряду с основным продуктом моноприсоединения получается хлорид с олефиновой структурой. [13]
При гемолитическом присоединении алкантиолов к триалкилэтинил-германам выход продуктов моно - и диприсоединения зависит от соотношения реагентов. Увеличение объема заместителей при атоме германия и увеличение разветвленное алкнльной группы в исходном меркаптане повышает выход продуктов моноприсоединения и снижает выход продуктов диприсоединения. [14]
Реакции оловоорганических гидридов с диинами проходят ступенчато. Из гидрида триметилолова и 1 8-нонадиина получают [27] ( СНз) 35пСНСН ( СН2) 5СНСН8п ( СН3) 3 наряду с примесью ( - 5 %) ( CH3) sSnCHCH ( СН2) 5С [ Sn ( CH3) S ] CH2 и очень небольшого количества продукта моноприсоединения. [15]
Страницы: 1 2