Моноселениды
Cтраница 2
Все моноселениды лантаноидов и актиноидов, за исключением Eu, Yb, Sm и, вероятно, Тт имеют металлическую проводимость, у них сравнительно легко происходит переход f - электронов. Двухвалентные Eu, Yb, Sm и, по-видимому, Тт, имеющие достаточно прочно связанные на глубоком 4 / - уровне электроны, образуют соединения ионного типа с полупроводниковыми свойствами ( см. гл. Остальные валентные электроны оказываются свободными, чем объясняется их металлическая проводимость. [16]
Металлогидридным методом были получены моноселениды ла. Этим методом могут быть получены и другие моноселениды РЗМ иттриевой группы. [17]
Полученное в работе [1] соединение PtSe0l80 было идентифицировано как моноселенид; у него моноклинная решетка; а 6 5806 A, b 4 6248 А, с 11 145 А, р 78 40; точка плавления 1055 15 С. [18]
В работе [122], проводимой в Институте полупроводников АН СССР, моноселениды получали также синтезом из простых веществ, который состоял из двух последовательных процессов: 1) взаимодействия металла с парами халькогена в ампуле при температуре не выше 600 С и 2) высокотемпературного отжига до 2000 С и плавки. [19]
Для РЗЭ, особенно для элементов цериевой подгруппы, характерно разнообразие типов С. Моноселениды М8е наиб, тугоплавки, плавятся конгруэнтно выше 1500 С, С. С; с повышением содержания 8е т-ры плавления понижаются. Сесквиселениды М28е3 - полупроводники; для них характерен полиморфизм; легко разлагаются разб. Полиселениды обладают более металлич. [20]
Моноселениды La, Се, Рг и Nd чрезвычайно химически активные соединения - порошки легко окисляются на воздухе при обычной температуре. Моноселениды от Sm до Lu довольно устойчивые соединения ( в спрессованном состоянии относительно устойчивы), что объясняется образованием тончайшей пленки окиси лантаноида. На основании результатов исследования сделаны выводы о ионно-металлическом характере связи в моно-селенидах трехвалентных лантаноидов и ионно-ковалент-ной в сесквиселенидах и полиселенидах с увеличением ковалентной составляющей связи при переходе от сес-квиселенидов к полиселенидам. [21]
Моноселениды Се и 8п имеют ромбич. [22]
SnSe кристаллизуется в ромбической решетке, представляющей собой деформированную структуру NaCl. Моноселенид олова изоструктурен сульфидам германия и олова. [23]
В работе [121] было установлено, что пары селена при температуре 800 С реагируют с порошком металлического никеля, образуя поликристаллы кубической системы. Моноселенид никеля NiSe был получен Фонзес - Дьяконом [407] при взаимодействии никеля с парами селена, увлекаемыми током азота при 700 - 800 С; кристаллы имеют серый цвет с голубоватым оттенком. NiSe может быть получен при взаимодействии хлорида никеля с селеноводородом при температуре 11дО С. Полуторный селенид Ni2Se3 и Ni3Se4, по-видимому, как индивидуальные фазы не существуют. [24]
В возгонах обнаружен и селен, и металл. Получить моноселениды в чистом виде термическим разложением селенидов не возможно. Единственно приемлемым методом получения моноселенидов РЗМ является металлогидридный метод, описанный ранее. [25]
При 540 5 С моноселенид олова имеет фазовое превращение [173], являющееся, по предположению [174], переходом второго рода. [26]
Металлогидридным методом были получены моноселениды ла. Этим методом могут быть получены и другие моноселениды РЗМ иттриевой группы. [27]
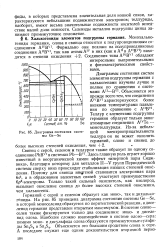 |
Диаграмма состояния системы Ge-Se. [28] |
Германий с серой и селеном образует как моно -, так и дихалько-гениды. На рис. 85 приведена диаграмма состояния системы Ge-Se, в которой моноселенид образуется по перитектической реакции, адисе-ленид германия представлен открытым максимумом. В системе олово - селен также фиксируются только два соединения: моно - и диселе-нид олова. Объясняется это большим сродством олова к сере. [29]
Сесквиселениды В и А1 неустойчивы, быстро гидролизуются водой; Са28е3 и 1п28е3 устойчивы, тогда ка1: Т128е3 разлагается при охлаждении. Моноселениды М8е известны для Са, 1п и Т1, причем у них либо присутствуют связи металл-металл, либо они представляют собой комплексы М1М 8е2; кристаллизуются в слоистых структурах. Са, а у остальных элементов - устойчивы только в парах. [30]
Страницы: 1 2 3