Монофторид - хлор
Cтраница 2
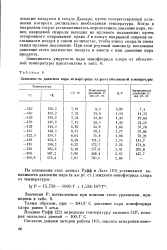 |
Зависимо. ть давления пара мснофтлрида хллра от абсолютной тзмпературы. [16] |
Таким образом, при - 100 8 С давление пара монофторида хлора равно 1 атм. [17]
В результате анализа литературных данных составлена сводка [32] ряда термодинамических характеристик газообразного монофторида хлора. [18]
К сожалению, исходя из этой величины, а также теплот диссоциации хлора и монофторида хлора, величина теплоты диссоциации фтора составляет 33 4 или 30 6 ккал. Эти значения настолько меньше обычно принятой величины теплоты диссоциации фтора ( 62 6 ккал), что для выяснения этого вопроса необходимы дальнейшие исследования. [19]
Если учитывать определенное Вартенбергом [24] значение теплоты образования фтористого водорода - 64 ккал, то теплота образования монофторида хлора равна 27 ккал. [20]
Шмитц и Шумахер [28] сообщили, что смешение трифторида хлора и хлора ведет к почти количественному образованию монофторида хлора. С тех пор как трифторид хлора стал промышленно доступен, последний способ получения монофторида хлора стал более удобен, чем способ синтеза из элементов. [21]
Трифторид хлора был получен в 1930 г. Руффом и Кру гом [11] в аппаратуре, ранее применявшейся для синтеза монофторида хлора. Фтор после электролизера проходил через медный цилиндр, заполненный фторидом калия для поглощения фтористого водорода, и через кварцевый сосуд, охлаждаемый до - 127 С. Этот сосуд служил для выделения хлора и фторуглеродов, которые могли образоваться на угольном аноде во фторной ванне. Очищенные фтор и хлор подавали в нагретый медный реактор. За реактором устанавливали три приемника, предназначенные для конденсации трифторида хлора, монофторида хлора и не вступившего в реакцию фтора. Первые два приемника были изготовлены из кварца, третий - из стекла. [22]
По реакционной способности галоидофториды можно расположить приблизительно в следующем порядке: трифторид хлора, пентафторид брома, гептафторид иода, монофторид хлора, трифторид брома, пентафторид иода, монофторид брома. Наиболее реакционноспособным является трифторид хлора. Большинство имеющихся в литературе данных относится только к качественной характеристике зтих веществ и в некоторых случаях не является достаточно удовлетворительным. Однако приведенные ниже данные дают некоторое представление о наиболее важных свойствах этих соединений. [23]
Для Константы Трутона найдена величина 30 6 кал - град-1 моль-1, что, по данным Гринвуда [23], свидетельствует об ассоциированной природе монофторида хлора в конденсированном состоянии. [24]
Если же за значение теплового эффекта реакции GIF F2 C1F3 принять недавно полученную [32] величину 24 50 ккал, а для теплоты образования монофторида хлора 13 4 ккал [14], то теплота образования трифторида хлора из элементов составит 37 9 1 0 ккал. [25]
Учитывая сказанное и принимая во внимание, что в большинстве случаев F выступает как отрицательная часть молекулы, естественно галоидные соединения фтора GIF, BrF, JF называть фторидами: соответственно монофторид хлора, брома, иода. Для соединений, в которых галогены имеют валентность выше единицы, следует сохранить тот же принцип, только перед словом фторид указать количество фтора в молекуле: C1F3, BrF5, JF - соответственно трифторид хлора, пентафторид брома, гептафторид иода. [26]
 |
Бинарные соединения хлора ( I. [27] |
Из бинарных соединений хлора ( I) относительно устойчив лишь C1F - слабо экзотермическое соединение. Монофторид хлора образуется при нагревании сухих С12 и F2 выше 270 С. Нитрид C13N и оксид С120 - эндотермические соединения и неустойчивы. [28]
Приготовление этого соединения затрудняется чрезвычайной агрессивностью соединения, которое реагирует со стеклом с образованием взрывчатых окислов хлора, а на металлы, включая мышьяк и сурьму, действует еще энер - гичнее, чем сам фтор. Монофторид хлора - почти бесцветный газ, который лишь при ильном охлаждении может быть переведен в жидкое и затем в твердое состояние. [29]
Приготовление этого соединения затрудняется чрезвычайной агрессивностью соединения, которое реагирует со стеклом с образованием взрывчатых окислов хлора, а на металлы, включая мышьяк и сурьму, действует еще энергичнее, чем сам фтор. Монофторид хлора - почти бесцветный газ, который лишь при сильном охлаждении может быть переведен в жидкое и затем в твердое состояние. [30]
Страницы: 1 2 3 4