Монохлорангидрид
Cтраница 1
Монохлорангидриды малеиновой и фумаровов кислот неизвестны. При нагревании фумаровой кислоты с пяти-хлористым фосфором или тионилхлоридом образуется хлористый фумароил. [1]
Монохлорангидриды моноэфиров и моноанилидов ацилами-дофосфорных кислот и хлорангидриды ациламидоарилфосфо-новых кислот - довольно высокоплавкие кристаллические вещества, трудно растворимые в обычных органических растворителях. [2]
Монохлорангидриды моноэфиров и моноанилидов ацилами-дофосфорных кислот и хлорангидриды ациламидоарилфосфоно-вых кислот гораздо более устойчивы к дальнейшему гидролизу, чем исходные фосфазосоединения. [3]
Монохлорангидриды эфиров дикарбоновых кислот могут быть переведены в; ответстяующие моноамиды эфирен дикарбоновых кислот с сохранением сложноэфа яой группы. [4]
Изучена кинетика реакции ацилирования анилина монохлорангидридом лг-карборанкарбоновой кислоты в метиленхлориде, 1 2-дихлор-этане, трихлорэтилене и тетрахлорэтилене при трех температурах. [5]
При использовании других соотношений реагентов можно получать монохлорангидриды, хотя препаративное значение такие превращения имеют редко. В то же время некоторые из этих реакций могут проходить селективно. [6]
Диметилмалоновую кислоту действием хлористого тионила переводят в монохлорангидрид, который при осторожном нагревании дает соответственный ангидрид. Последний при более энергичном нагревании отщепляет углекислоту и превращается в диметилкетен. [7]
Далее сульфирующими агентами служат хлорсульфоновая кислота ( монохлорангидрид серной кислоты) C1SO3H, некоторые вещества, могущие выделять серный ангидрид при реакциях, и - реже - сернистая кислота в виде солей ( при одновременном восстановлении заместителя, уже имеющегося) и иногда кислые соли серной кислоты. [8]
Наилучшие выхода получаются, если вести разложение монохлорангидрида в вакууме 12 мм при возможно более низкой температуре. При этом сначала жидкая масса выделяет хлороводо-род, постепенно густеет и под конец превращается в твердое желтое вещество. [9]
Образование карбоксилсодержащих соединений - 4-трихлорметилбензойной кислоты, терефталевой кислоты и ее монохлорангидрида можно объяснить тем, что скорость гидролиза соединений с COCl-группой в соединения с СООН-группой значительно превышает скорость гидролиза соединений с трихлорметильной группой. [11]
При действии на рибофлавин различных фосфорилирующих агентов, в качестве которых применяют хлорокись фосфора, монохлорангидрид ортофосфорной кислоты, хлорангидриды диалкилзамещенных ортофосфор-ной кислоты, реагирует первичная гидроксильная группа и образуется ри-бофлавин-5 - фосфат ( V) [29 - 37], а также другие эфиры - ди - и поли-5 - фосфаты рибофлавина. [12]
На первом этапе трихлорид превращается в алкилдихлортионфосфаты с выходом около 90 %; при вторичном фосфорилировании образуется монохлорангидрид уже с меньшим выходом. [13]
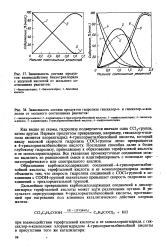
Как видно из данных табл. 3, при обработке ЦЭЦ дихлорангидридами фенилфосфорной и метилфосфоновой кислот прочность падает незначительно, а в случае монохлорангидрида фенилфосфорной кислоты она практически сохраняется. [14]
ДМФА быстро и количественно реагирует с тионилхлоридом, образуя ионный комплекс К - На первой равновесной стадии анион хлора ионного комплекса К атакует карбонильный атом углерода ангидридного цикла, давая монохлорангидрид ионного комплекса структуры АК - Последний в лимитирующей стадии взаимодействует с молекулой тионилхлорида, образуя монохлорангидрид нестойкого смешанного ангидрида структуры С, который быстро элиминирует диоксид серы, давая ортодихлорангидрид. Таким образом, ионный комплекс К выполняет роль катализатора. [15]
Страницы: 1 2