Монохлорангидрид
Cтраница 2
Поскольку соединения XIII получают сложным синтезом и последующий ряд превращений представляет некоторые трудности, заслуживает большого внимания синтез макроцикличе-ских кетонов внутримолекулярным ацилированием хлорангидри-дов со - ( тиенил-2) - алкановых кислот, получаемых из тиофена н монохлорангидридов двухосновных кислот или из тиофена и хлорангидридов - хлоралкановых кислот, ставших в последнее время доступными благодаря освоению производства продуктов теломеризации этилена с четыреххлористым углеродом. [16]
ДМФА быстро и количественно реагирует с тионилхлоридом, образуя ионный комплекс К - На первой равновесной стадии анион хлора ионного комплекса К атакует карбонильный атом углерода ангидридного цикла, давая монохлорангидрид ионного комплекса структуры АК - Последний в лимитирующей стадии взаимодействует с молекулой тионилхлорида, образуя монохлорангидрид нестойкого смешанного ангидрида структуры С, который быстро элиминирует диоксид серы, давая ортодихлорангидрид. Таким образом, ионный комплекс К выполняет роль катализатора. [17]
Как показано С. В. Соколовской и О. Ю. Магидсоном, бигуаниды, полученные из замещенных анилинов п дициандиамида, вступая в реакцию с эфирами одноосновных кислот, легко образуют 2-амнио - 4 - К-135 - триазины. Если применить монохлорангидрид двухосновной кислоты, то образуются эфиры замещенной 2 4-диамино - 1 3 5-триазол - 6-алкилкарбоновой кислоты. [18]
С, остаток экстрагирован петролейньш эфиром, экстракт обработан активированным углем, упарен более чем наполовину, охлажден до 0 С. Через некоторое время отфильтрован монохлорангидрид. [19]
В чистом виде это интересное соединение выделено не было, однако было показано, что при реакции с анилином оно дает ожидаемое соединение C6H5NHCOCH2S03H, выделенное в виде анилиниевой соли. Несомненно, что перспектива применения указанного ангидрида заслуживает внимательного рассмотрения, поскольку она открывает прямой и недорогой путь получения производных сульфоуксусной кислоты, имеющих ту же структуру, что и вещества, получаемые исходя из обсуждавшегося выше монохлорангидрида. [20]
 |
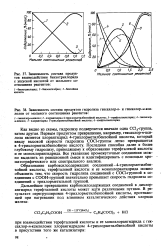
Фор минирование ароматических соединений с помощью различных электрофнльных агентов. [21] |
Сульфирование широко используется в промышленном органическом синтезе для получения промежуточных продуктов в промышленности органических красителей, а также для синтеза поверхностно-активных веществ, сульфамидных препаратов и других физиологически активных соединений. В качестве сульфирующего агента чаще всего употребляют 98 - 100 % - ю серную кислоту ( моногидрат), 92 - 94 % - ю серную кислоту ( купоросное масло), а также олеум, содержащий от 20 до 60 % серного ангидрида, растворенного в безводной серной кислоте; иногда для сульфирования используют растворы 8Оз в SC2 и 8Оз в хлористом метилене. Эффективным сульфирующим агентом является хлорсульфоновая кислота ( монохлорангидрид серной кислоты), которую получают при взаимодействии серного ангидрида и хлористого водорода. Сульфирование ароматических соединений хлорсульфоновой кислотой представляет собой двухстадийный процесс. [22]
Сульфирование широко используется в промышленном органическом синтезе для получения промежуточных продуктов в промышленности органических красителей, а также для синтеза поверхностно-активных веществ, сульфамидных препаратов и других физиологически активных соединений. В качестве сульфирующего агента чаще всего употребляют 98 - 100 % - ю серную кислоту ( моногидрат), 92 - 94 % - ю серную кислоту ( купоросное масло), а также олеум, содержащий от 20 до 60 % серного ангидрида, растворенного в безводной серной кислоте; иногда для сульфирования используют растворы SO3 в SO2 и SO3 в хлористом метилене. Эффективным сульфирующим агентом является хлорсульфоно-вая кислота ( монохлорангидрид серной кислоты), которую получают при взаимодействии серного ангидрида и хлористого водорода. Сульфирование ароматических соединений хлорсульфоно-вой кислотой представляет собой двухстадийный процесс. [23]
Как видно из схемы, гидролизу подвергается вначале одна СС13 - группа, затем другая. Первым продуктом превращения, например, гексахлор-п-кси-лола является хлорангидрид 4-трихлорметилбензойной кислоты, который ввиду высокой скорости гидролиза COCl-группы легко превращается в 4-трихлорметилбензойную кислоту. Последняя способна далее к более глубокому гидролизу, приводящему к образованию терефталевой кислоты и ее монохлорангидрида. [25]
Вторая стадия формолиза идет только в кипящем бензоле и длится от 30 мин до полутора часов. Растворимость продуктов второй ступени ацидолиза трихлорфосфазосульфонилов значительно меньше растворимости дихлорангидридов сульфонилами-дофосфорных кислот. Поэтому они выпадают из раствора в виде кристаллического осадка или в виде масла, которое часто удается закристаллизовать. Иногда монохлорангидриды выпадают очень медленно - в течение 2 - 3 суток. [26]
Страницы: 1 2