Диаллилдиан
Cтраница 1
Диаллилдиан благодаря наличию аллильной группы может быть использован для сшивания линейных макромолекул поликарбонатов. Их можно использовать для получения покрытий, высыхающих на воздухе или спекающихся в печах, а также как литьевые или формующиеся материалы. Если содержание диаллилдиана в таком смешанном полимере не превышает 10 мол. [1]
Значительная растворимость фенолята диаллилдиана в re - ксилоле позволяет предполагать, что часть полиамидоарилата, синтезируемого межфазной поликонденсацией на основе этого двухатомного фенола, будет получаться и в органической фазе. На основе приведенных выше данных, по-видимому, можно предположить, что полиамидоарилат образуется в зоне соприкосновения двух фаз, включая границу раздела фаз и некоторую область каждой из фаз. Ширина этой области будет обусловлена химической природой реагирующих веществ и растворителей. [2]
Когда же в межфазпой поликонденсации молярное соотношение хлорангид-рид кислоты: диан: диаллилдиан составляло 1 0: 1 0: 2 0 моля, получался только гомополиарилат диаллилдиана. [3]
В соответствии с этими уравнениями энергия активации поликонденсации хлорангидрида изофталевой кислоты с диаллилдианом составляет 18 900 кал / моль, фактор вероятности равен 0 247 - 10 л / молъ-сек. Энергия активации поликонденсации хлорангидрида терефталевой кислоты с диаллилдианом равна 18600 кал / моль, фактор вероятности - 0 196 - Ю6 л / моль-сек. Если сопоставить эти величины с приведенными выше значениями по энергии активации и фактору вероятности для поликонденсации соответствующих хлор-ангидридов дикарбоновых кислот с 4 4 -диоксидифенил - 2.2 - пропаном ( диа-ном), то можно видеть, что введение в молекулу данного двухатомного фенола двух боковых аллильных групп способствует уменьшению энергии активации и фактора вероятности. [5]
Уменьшение частоты столкновения хлорангидридных групп с гидрок-сильными при поликонденсации хлорангидридов терефталевой и изофталевой кислот с диаллилдианом, по-видимому, связано с пространственным эффектом, проявляющимся в экранировании гидроксильных групп двухатомного фенола аллильнъши радикалами. Такое экранирование в случае диаллилдиана и создает большее препятствие к приближению хлорангидридной группы мономера ими растущей цепи к гидроксильной группе, чем это имеет место при использовании в качестве двухатомного фенола диана. [6]
Если же сравнивать между собой степени завершенности реакции хлор-ангидридов ароматических дикарбоновых кислот с дианом и диаллилдианом ( рис. 43), то следует отметить более медленное течение процесса в случае диаллилдиана. [7]
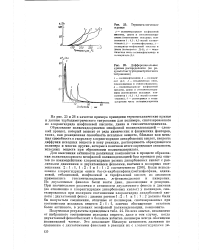
В табл. 59 и на рис. 42, а и б приведены данные о степенях завершенности реакции взаимодействия диаллилдиана с хлорангидридами терефталевой и изофталевой кислот при различных температурах и продолжительности ре-акции. Из рис. 42 видно, что степень завершенности данных реакций заметно возрастает с увеличением температуры реакции, причем более половины всего хлористого водорода, выделившегося в ходе реакции, приходится на первые 2 - 3 часа протекания поликонденсации. В дальнейшем наблюдается более медленное возрастание степени завершенности реакции. [8]
Когда же в межфазпой поликонденсации молярное соотношение хлорангид-рид кислоты: диан: диаллилдиан составляло 1 0: 1 0: 2 0 моля, получался только гомополиарилат диаллилдиана. [9]
В табл. 59 приведены константы скоростей и степени завершенности реакций при поликонденсации хлорангидридов терефталевой и изофталевой кислот с 4 4 -диокси - 3 3 -диаллилдифенил - 2 2-пропаном ( диаллилдианом) в среде динила для интервала 180 - 220 С. [10]
Если же сравнивать между собой степени завершенности реакции хлор-ангидридов ароматических дикарбоновых кислот с дианом и диаллилдианом ( рис. 43), то следует отметить более медленное течение процесса в случае диаллилдиана. [11]
 |
Влияние различных добавок на рост цепи ( изменение молекулярного веса полиэфира. [12] |
Виноградова, Коршак и Корчевей [281, 282] для получения ненасыщенных полиэфиров невысокого молекулярного веса, не содержащих на концах цепи фенольных ОН-групп, проводили поликонденсацию хлорангидри-да изофталевой или терефталевой кислоты ( взятых в небольшом избытке) с фенолфталеином и диаллилдианом, добавляя на втором этапе процесса к реакционной смеси монофункциональное вещество - 2-аллилфенол. [13]
Уменьшение частоты столкновения хлорангидридных групп с гидрок-сильными при поликонденсации хлорангидридов терефталевой и изофталевой кислот с диаллилдианом, по-видимому, связано с пространственным эффектом, проявляющимся в экранировании гидроксильных групп двухатомного фенола аллильнъши радикалами. Такое экранирование в случае диаллилдиана и создает большее препятствие к приближению хлорангидридной группы мономера ими растущей цепи к гидроксильной группе, чем это имеет место при использовании в качестве двухатомного фенола диана. [14]
 |
Дифференциальные кривые распределения ( по результатам турбодиметрического титрования. [15] |
Страницы: 1 2
