Накагава
Cтраница 1
Накагава и Курияма [10] развили теорию, в соответствии с которой главными факторами, препятствующими ассоциации, являются теплота гидратации и конформационная энтропия гибкой гидрофильной цепи. Эта теория позволяет количейт-венно предсказывать величину ККМ, мицеллярного веса и других характеристик раствора, но не в состоянии удовлетворительно объяснить влияние на них температуры и явление помутнения. [1]
Накагава с сотрудниками [34] измерили мицеллярные веса очищенных метоксиполиоксиэтиленкапринатов и метоксиполиок-сиэтиленлауратов. В этих расчетах значения ККМ ( 2 - К) - 4 - 18 - Ю моль / л), определенные по солюбилизации Судана III, вычитались из стехиометрических концентраций. [2]
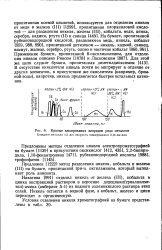 |
Кривые элюирования хлоридов ряда металлов. [3] |
Накагава [991] отделил никель от железа ( III), кобальта и цинка экстракцией раствором в керосине додецинил ( триалкилме-тил) - амина ( амберлит А-1) из водного солянокислого раствора этих солей. Никель остается в водной фазе, а кобальт, железо и цинк переходят в органическую. [4]
Накагава [89] рекомендует следующий простой метод разделения и определения олова и свинца. [5]
Накагава и Курияма [10] развили теорию, в соответствии с которой главными факторами, препятствующими ассоциации, являются теплота гидратации и конформационная энтропия гибкой гидрофильной цепи. Эта теория позволяет количественно предсказывать величину ККМ, мицеллярного веса и других характеристик раствора, но не в состоянии удовлетворительно объяснить влияние на них температуры и явление помутнения. [6]
Накагава и Курияма [5] предложили теорию ассоциации молекул неионогенных ПАВ, в которой основным фактором, препятствующим ассоциации молекул, является теплота гидратации полярных групп и конформационные изменения энтропии гибкой гидрофильной цепи молекулы ПАВ. [7]
Накагава с сотрудниками [34] измерили Мицеллярные веса очищенных метоксиполиоксиэтиленкапринатов и метоксиполиок-сиэтиленлауратов. В этих расчетах значения ККМ ( 2 - 10 - 4 - 18 - Ю 4 моль / л), определенные по солюбилизации Судана III, вычитались из стехиометрических концентраций. [8]
Мидзусима и Накагава [76] приводят рассчитанную ими диаграмму ( рис. 8), изображающую зависимость частот маятниковых колебаний симметрии А и В от угла внутреннего вращения. К сожалению, малая интенсивность полос поглощения, отвечающих колебаниям QCH, часто препятствует их использованию в качестве структурного критерия. Такого рода трудности встречаются, в частности, при интерпретации спектров циклических этилендиаминовых комплексов. [9]
Мидзусима, Накагава и их сотрудники [139,146] произвели довольно детальный расчет частот и силовых постоянных деформаций групп NH2 в зигзагообразной цепи - NH2 - Hg - NH2 - Hg - в этих веществах. Полученные ими экспериментальные данные находятся в основном в согласии с данными Накагава и сотрудников, но убедительный анализ, произведенный последними авторами, показал, что некоторые из отнесений, данных Бродерсеном и Бехером, неправильны. [10]
В работе Накагавы и Шиманоучи251 измеренные значения - постоянных для молекулы CH3CN дополнены расчетными. [11]
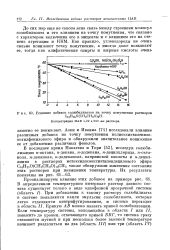 |
Влияние добавок солюбилизатов на точку помутнения растворов. [12] |
В последнее время Накагава и Тори [52], исследуя солюби-лизацию к-октана, w - декана, к-додекана, к-децилхлорида, к-окта-нола, н-деканола, к-додеканола, каприновой кислоты и к-децил-амина в растворах метоксидекаоксиэтилендецилового эфира С1оН210 ( СН2СНоО) 1оСНз также обнаружили изменение состояния этих растворов при повышении температуры. [13]
Недавно Симаноути и Накагава [ 16а ] провели анализ нормальных колебаний иона [ Со ( МН3) б ] 3, рассматривая NHs-группу как один атом. [14]
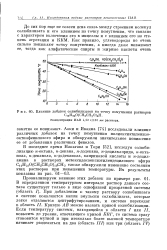 |
Влияние добавок солюбилизатов на точку помутнения растворов. [15] |
Страницы: 1 2 3