Накопление - атом - хлор
Cтраница 2
Сравнение условий замены хлора на оксигруппу в хлорбензоле и полпхлорпронзводных бензола отчетливо показывает, что по мере накопления атомов хлора в бензольном кольце подвижность галоида увеличивается. [16]
Сравнение условий замены хлора на оксигруппу в хлорбензоле и полихлорпроизводных бензола отчетливо показывает, что по мере накопления атомов хлора в бензольном кольце подвижность галоида увеличивается. [17]
Хлорированные хлоругольные и угольные эфиры обладают удушливым запахом и лакримогенными свойствами, убывающими по мере увеличения количества атомов хлора в радикалах; наоборот, их токсические свойства с накоплением атомов хлора усиливаются. [18]
Для процессов дегидрохлорирования ( реакции 1, 2, 3) большему смещению равновесия вправо способствует нахождение атома хлора не у первичного, а у третичного ( и вторичного) углеродного атома и накопление атомов хлора в молекуле, в особенности при одном и том же углеродном атоме. [19]
Хлорированные хлоругольные эфиры не только слезоточивые, но и удушающие вещества. Слезоточивое действие уменьшается с накоплением атомов хлора в молекуле, а удушающее действие увеличивается. [20]
Как известно, при накоплении связей CF во фторметанах или при двух атомах углерода во фторэтиленах происходит заметное укорочение всех связей, образованных атомами углерода. Менее ярко этот эффект проявляется при накоплении атомов хлора. Эти факты представляли крепкий орешек для теоретиков, и объяснения со ссылкой только на гибридизацию или только на влияние разницы в электроотрицательностях атомов фтора и углерода не были достаточно удовлетворительны. Питере комбинирует оба эти соображения. Атом фтора оттягивает на себя ( withdraw) электроны от атома углерода. Поэтому, чем больше атомов фтора соединено с данным атомом углерода, тем больший положительный заряд приобретает последний. [21]
Алкил -, N-алкил -, N-арил -, 8-арил - 1Ч - алкиламидоалкилтиофосфонаты обладают слабым фитотоксическим действием. В рядуО - арил - М - алкиламидофос фонатов и тиофосфонатов накопление атомов хлора до двух приводит к повышению гербицидной активности соединений. Наиболее токсичны для растений 0 - 4-хлорфенилыше и 0 - 2 4-дихлорфенильные производные. Переход к 0 - 2 4, 5-трихлорфенил - и 0-пентахлорфениламидоалкилфосфонатам и тиофосфонатам сопровождается обращением активности от гербицидной к фунгицидной. [22]
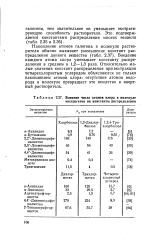 |
Влияние числа атомов хлора в молекуле экстрагента на константы распределения. [23] |
Введение каждого атома хлора уменьшает константу распределения в среднем в 1 2 - 1 3 раза. Относительно малые значения констант распределения при экстракции четыреххлориетым углеродом объясняются не только накоплением атомов хлора: отсутствие атомов водорода в молекуле превращает это вещество в инертный растворитель. [24]
Продолжительность реакции варьировали от 15 до 300 мин. Отмечено лишь очень незначительное ослабление связи С - С1 в ароматической системе, вызванное накоплением атомов хлора. В растворе щелочи в этиловом спирте вообще не происходит отщепления хлора, а в растворе в пропиловом спирте максимальное отщепление составляло меньше 1 % от общего содержания хлора. Повышение температуры при работе с раствором в бутиловом и в циклогексиловом спирте приводит к отщеплению не более 10 % хлора. [25]
В принципе любая С - С1 - связь может быть превращена в С - Н - связь, однако легкость и избирательность восстановления сильно зависит от строения хлорсодержащей функциональной группы, от наличия и расположения в молекуле других функциональных групп, от природы восстановителя. Так, например, обычно хлор у винильного атома углерода замещается на водород труднее, а у аллильного легче, чем в предельных хлоруглеводородах. Накопление атомов хлора или других электроноакцепторных групп у углеродного атома, связанного с хлором, облегчает восстановление. Атом хлора, находящийся в а-положении к электроноакцепторной группе, замещается легче, чем более отдаленные атомы хлора в той же молекуле. [26]
Очевидно, здесь значительную роль играет эффект сопряжения связи Si-С и связей С - Н р-атома углерода. Неспаренный электрон образующегося в реакции свободного радикала ( С2Н5) з51СН2СН2 -, находясь в сопряжении с атомом кремния, стабилизируется и становится не способным к продолжению цепи. С накоплением атомов хлора у атома кремния величина эффекта сопряжения уменьшается и хлорирование в этилхлорсилане определяется, вероятно, уже только индуктивным и пространственным эффектами. [27]
Приведенные в табл. 14 соединения по своим свойствам в значительной мере сходны с 1 2 3 4 5 6-гексахлорциклогексаном. Это-кристаллические вещества, растворимые в органических растворителях. Растворимость их уменьшается по мере накопления атомов хлора, связанных с кольцом углеродных атомов. [28]
Введение атома хлора в геминаль-ное положение, с одной стороны, уменьшает энергию диссоциации связи С - Н, что должно облегчать отрыв атома - водорода и, следовательно, увеличивать скорость реакции по мере накопления атомов хлора при реакционном центре. [29]
Токсичность эфиров резко возрастает при переходе от соединений алифатического ряда к соединениям ароматического ряда. Особенно токсичны эфиры, содержащие в ароматическом радикале различные функциональные группы или галоиды. Так, например, 2 4-динитроанизол обладает настолько сильным инсектицидным действием, что в течение ряда лет применялся в армии США для борьбы с педикулезом. Хлоранизолы также являются сильными инсектицидами, их активность возрастает с накоплением атомов хлора в молекуле. [30]
Страницы: 1 2 3