Наличие - ароматическое кольцо
Cтраница 1
Наличие ароматического кольца дает возможность применить УФ-спектроскопию. [1]
Наличие ароматического кольца отрицательно влияет на степень деструкции сульфидов; так, фенилгексилсульфид за 7 сут. [2]
Однако наличие ароматического кольца создает некоторые особые возможности идентификации с помощью спектров. Типичные ИК - и ПМР-спектры анилинов приведены на рис. 6.18 и 6.19 соответственно. Практически все описанные ниже методы получения производных аминов могут быть использованы для получения производных анилинов. [3]
Пероксидации способствует наличие ароматического кольца, а также двойной связи; при этом атака кислорода направляется на ближайшую к ним алифатическую или алициклическую С - Н связь. [4]
Считается, что наличие ароматических колец в молекуле пластификатора нежелательно. Стевенсон, Чейни и Болдуин150 исследовали пригодность тетрахлорфталевой кислоты в качестве исходного вещества для получения пластификаторов. [5]
Водород насыщенного кольца тетралина активизируется наличием смежного ароматического кольца. [6]
Механические свойства полиэфирных волокон определяются наличием жестких ароматических колец. Они достаточно прочны, но менее эластичны, хуже выдерживают многократные деформации и легче истираются, чем полиамидные волокна. Модуль деформации и жесткость этих волокон по тем же причинам значительно выше, чем у полиамидных. [7]
Химические свойства бензола и его гомологов обусловлены наличием ароматического кольца. [8]
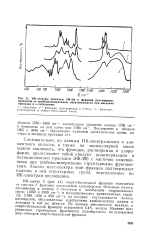 |
ИК-спектры присадки ЭФ-390 и фракций растворимых продуктов ее трибополимеризации, образовавшихся при введении присадки в н-тетрадекан. [9] |
Поглощение в области 1605 и 3045 см-1 обусловлено наличием ароматических колец, которых в молекуле присадки нет. [10]
Полосы 1605, 848 и 759 см - позволяют предположить наличие ароматического кольца. Полоса 1380 см 1 появляется за счет метальной группы. Так определяется метилпиридин карбоновая кислота; тип замещения из спектра неясен. [11]
ДДХ часто служит наилучшим реагентом для дегидрирования углеводородов, активированных наличием ароматического кольца или двойной связи. [12]
Приведенное расположение исследованных сульфидов в ряд по относительным скоростям гидрогенолиза интересно именно тем, что наличие ароматических колец в сульфидах обусловливает большие относительные скорости гидрирования. Например, дифенилсульфид гидрируется почти в два раза с большей относительной скоростью но сравнению с диэтилфепилсульфидом. Объяснить это чисто адсорбционными явлениями нельзя, хотя очевидно, что адсорбция играет значительную роль при гидрогенолизе в жидкой фазе. [13]
Приведенное расположение исследованных сульфидов в ряд по относительным скоростям гидрогенолиза интересно именно тем, что наличие ароматических колец в сульфидах обусловливает большие относительные скорости гидрирования. Например, дифенилсульфид гидрируется почти в два раза с большей относительной скоростью ло сравнению с диэтилфенилсульфидом. Объяснить это чисто адсорбционными явлениями нельзя, хотя очевидно, что адсорбция играет значительную роль при гидрогенолизе в жидкой фазе. [14]
 |
Энергии разрыва связи С-Я ( & Н, параметры Аррениуса ( А, Е и относительные скорости ( г гемолитического бромирования циклоалканов. [15] |
Страницы: 1 2 3 4