Наличие - ионная атмосфера
Cтраница 1
Наличие ионных атмосфер препятствует выходу ионов из раствора, вследствие чего уменьшается осмотическое давление. Именно поэтому измеренное осмотическое давление ( я) меньше того ( я), которое раствор имел бы, если бы частицы растворенного вещества не имели зарядов. [1]
Наличие ионной атмосферы обусловливает величину электропроводности и. [2]
Наличие ионной атмосферы действует на электропроводность раствора в двух направлениях. Положительный ион окружен слегка отрицательной ионной атмосферой. При быстром движении положительного иона создается некоторый разрыв во времени между нейтрализацией отрицательной атмосферы позади иона и созданием положительной атмосферы впереди него, в результате чего возникает задерживающая сила. Запаздывание увеличивается с концентрацией, что приводит к уменьшению электропроводности при больших концентрациях, которое Аррениус относил за счет меньшей степени диссоциации. [3]
Таким образом, из-за наличия ионной атмосферы при движении иона возникают два тормозящих эффекта: электрофоретический, обусловленный движением ионной атмосферы в сторону, противоположную направлению движения иона, и эффект релаксации обусловленный асимметрией ионной атмосферы. [4]
Потенциал V k обусловлен наличием ионной атмосферы. [5]
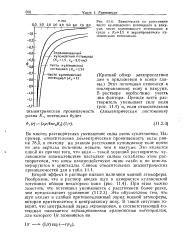 |
Зависимость от расстояния чисто кулоиовского потенциала в вакууме, чисто ку. чоновского потенциала в среде с / ( г и экранированного ку-лоновского потенциала. [6] |
Второй эффект в растворе вызван наличием ионной атмосферы. Это обусловлено тем, что щуп входит в слабый противоположный заряд ионной атмосферы, которая притягивается к центральному нону. [7]
В растворах электролитов этот порядок может быть описан как наличие ионных атмосфер вокруг каждого иона. [8]
Второй член этого уравнения a Y характеризует уменьшение электропроводности вследствие взаимного торможения ионов, природа которого обусловлена наличием ионных атмосфер, окружающих все находящиеся в растворе ионы. Различают два типа ионного торможения: электрофоретическое и релаксационное. [9]
Следует ожидать, что эффект Вина будет проявляться сильнее всего в таких условиях, когда влияние межионных сил, обусловленных наличием ионной атмосферы, особенно велико; это имеет место для концентрированных растворов многовалентных ионов. На рис. 36 приведены кривые для электролитов с разными типами валентности, причем растворы этих электролитов обладают одинаковыми электропроводностями при низком напряжении. ДА представляет собой увеличение эквивалентной электропроводности под влиянием наложения градиента потенциала, отложенного по оси абсцисс. [10]
В этой теории, помимо силы торможения иона, возникающей при его движении в вязкой среде, учитываются две дополнительные силы торможения, вызываемые наличием ионной атмосферы. Эти две силы связаны с двумя эффектами: электрофоретическим и релаксационным. [11]
Убедительным подтверждением правильности представлений Дебая и Гюккеля является так называемый эффект Вина, обнаруженный в 1927 г. Если уменьшение подвижности ионов с увеличением концентрации объясняется наличием ионной атмосферы, то уничтожение последней должно привести к возрастанию подвижности, а следовательно, и электропроводности до предельного значения. Поскольку скорость движения иона пропорциональна напряжению, а скорость образования ионной атмосферы является конечной величиной, то, очевидно, путем увеличения напряженности можно добиться такой большой скорости движения ионов, при которой ионная атмосфера уже не будет успевать образовываться. Тогда, покинув свои ионные атмосферы ( которые немедленно разрушаются), ионы будут двигаться уже без них, а следовательно, будут обладать максимальной скоростью движения и предельной подвижностью. Это и было установлено Вином, который увеличив напряженность поля 200 000 в / см, наблюдал увеличение эквивалентной электропроводности до предельного значения Ясс. [12]
В основу этой теории положена модель раствора, согласно которой каждый ион окружен преимущественно противоположно заряженными ионами, располагающимися вокруг данного центрального иона в виде сферы, называемой ионной атмосферой. Реальные растворы от идеальных отличаются наличием ионных атмосфер, эффект действия которых на центральные ионы выражается энергией межионного взаимодействия. [13]
 |
Зависимость удель ной электрической проводимости некоторых электроли тов от концентрации.| Удельная электрическая проводимость 0 1 М KCI при различных температурах. [14] |
Наличие х См / м максимумов на кривых объясняется тем, что в разбавленных растворах сильных электролитов скорость движения ионов почти не зависит от концентрации и к растет почти прямо пропорционально числу ионов, которое, в свою очередь, увеличивается с концентрацией. При достижении определенной концентрации в растворах сильных электролитов скорость движения ионов существенно уменьшается из-за наличия ионной атмосферы, в результате чего х также уменьшается. [15]
Страницы: 1 2