Наличие - свободный орбиталь
Cтраница 1
Наличие свободных орбиталей ( 3d) создает различие в свойствах элементов 2-го и 3-го периодов. [1]
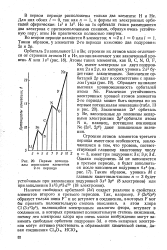 |
Первые потенциалы ионизации элементов 2-го периода. [2] |
Наличие свободных орбиталей ( 3d) создает различие в свойствах элементов второго и третьего периодов. [3]
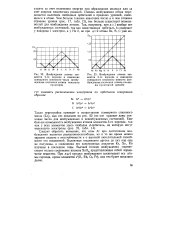
Степень возбуждения атома определяется наличием свободных орбиталей в пределах уровней, имеющихся в атоме. Чем больше главное квантовое число и чем сложнее строение уровня ( рис. 17, табл. 12), тем больше существует возможностей для возбуждения атомов. [5]
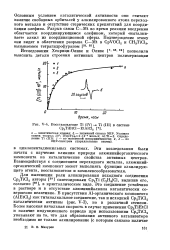 |
Восстановление Ti ( IV - Cp2TiEtCl - EtAlCL. [6] |
Основным условием каталитической активности они считают наличие свободных орбиталей у алкилированного атома переходного металла и отсутствие стерических препятствий для координации олефина. Разрыв связи С-Mt во время реакции внедрения облегчается координирующимся олефином, который выталкивает алкил из координационной сферы. [7]
I группы - солеобразные соединения, но при наличии свободных орбиталей у атомов, вступивших в соединение, легко переходят в комплексные соединения. [8]
Галиды d - металлов I группы - солеобразные соединения, но при наличии свободных орбиталей у атомов, вступивших в соединение, легко переходят в комплексные соединения. [9]
 |
Схема перекрывания орбиталей при образовании о -, л - и 6-связей. [10] |
Рассмотренные примеры показывают, что способность атома образовывать ковалентные связи обусловливается не только одно-электронными, но и двухэлектронными облаками или соответственно наличием свободных орбиталей. [11]
Рассмотренные примеры показывают, что способность атома образовывать ковалентные связи обусловливается не только одноэлектрон-ными, но и двухэлектронными облаками или соответственно наличием свободных орбиталей. [12]
Атом алюминия отличается от атома бора наличием свободного d - подуровня во внешнем слое, что создает возможность увеличения числа донорно-акцепторных связей. Наличием свободных орбиталей во внешнем электронном слое обусловлена склонность соединений бора и алюминия к полимеризации и реакциям присоединения. [13]
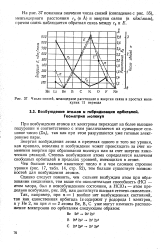 |
Число связей, межядерное расстояние и энергия связи в простых молекулах II периода. [14] |
Энергия возбуждения атома в пределах одного и того же уровня, как правило, невелика и возбуждение может происходить за счет изменения энергии при образовании молекул или за счет энергии химических реакций. Степень возбуждения атома определяется наличием свободных орбиталей в пределах уровней, имеющихся в атоме. [15]
Страницы: 1 2