Наличие - неподеленная пара - электрон
Cтраница 1
Наличие неподеленной пары электронов или же тс-свяэей по соседству с радикальным центром в радикале спосббствует наибольшей термодинамической стабильности радикала. Орбитальное взаимодействие в этом случае ( рис. 1, а) приводит к существенному выигрышу энергии. [1]
Наличие неподеленной пары электронов играет большую поль в определении формы молекул. Это видно из того обстоятельства что молекула ВН3 плоская, а ЫН3 - - пирамидальная. Поэтому следует заранее ожидать, что молекула ВеН, - окажется линеи-штй а ОН - изогнутой. Наличие неподеленной пары электронов v центрального атома приводит к резкому изменению конфигурации молекула изгибается таким образом, как будто электроны, обоазующие связи, начинают отталкиваться. [2]
Наличие неподеленной пары электронов в кислороде гид-роксильной группы обусловливает своеобразие диссоциативной ИОНИЗации молекулы спирта; вместе с тем определенную роль продолжает играть строение углеводородной цепи. [3]
Наличие неподеленной пары электронов обусловливает высокую донорную активность нитрит-иона как лиганда и его способность к образованию устойчивых комплексных соединений. [4]
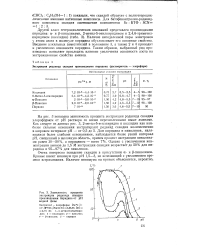 |
Зависимость процента экстракции роданида скандия производными пиридина от рН водной фазы. [5] |
Наличие неподеленной пары электронов у атома азота в молекуле пиридина обусловливает его основные свойства. Введение алкильных заместителей в положение 3, а также 2 и 4 приводит к увеличению основности пиридина. Таким образом, выбранный ряд производных позволяет проследить влияние увеличения основности азота на экстракционные свойства аминов. [6]
Наличие неподеленной пары электронов у фосфора обусловливает способность тригалогенидов проявлять донорные свойства. [7]
Наличие неподеленной пары электронов на сере, обеспечивающее возможность образования тиониевых ионов, определяет основной распад производных тиолана. [8]
Наличию неподеленной пары электронов обязана своим существованием и так называемая водородная связь. Она образуется между молекулами, содержащими электроотрицательные атомы ( О, N, F, реже Q, Вг, S), которые имеют свободную электронную пару, и молекулами с активными атомами водорода. [9]
Благодаря наличию неподеленной пары электронов пропионовая кислота склонна акцептировать ионы водорода и способна образовывать координационные связи. [10]
Амины, вследствие наличия неподеленной пары электронов у атомов азота, обладают донорными свойствами и в водных растворах способны образовывать положительно заряженные частицы. В кислых растворах этот процесс облегчается. Несомненно, на донорные свойства азота в амине влияет природа углеводородного радикала и атомов, находящихся в непосредственной близости к азоту. Это определяет химические и физические ( в данном случае адсорбционные) свойства соединений, содержащих трехвалентный азот. [11]
В случае нитритов наличие дополнительной неподеленной пары электронов на атоме азота приводит к уменьшению разности энергий между двумя конфигурациями III и IV, так что эти конфигурации могут сосуществовать. Это объяснение не учитывает большие различия ( до 60 см-1) между значениями vNO для двух форм. Если эта разность целиком определяется различиями в силах отталкивания неподеленных пар, то эти различия слишком велики. Положение еще более усложняется, так как по предварительным данным связь NO ыс-метилнитрита менее основная, чем у трансизомера, несмотря на то что транс-изомер характеризуется более высокой частотой колебаний, откуда можно было бы предполагать, что он менее полярен. Вполне вероятно, что измерения основности различных систем X-NO могут привести к объяснению свойств неподеленных пар электронов и благодаря этому к объяснению особенностей расположения самих связей. [12]
Основные свойства аммиака обусловлены наличием неподеленной пары электронов у атома азота. [13]
Такое увеличение нуклеофильности связано с наличием неподеленной пары электронов у сс-атома по отношению к атому - нуклеофилу ( см. стр. [14]
Общим для указанных случаев ненормального гидролиза является наличие неподеленной пары электронов у атома соседнего с углеродным атомом, несущим сульфогруппу. Переход электронной пары на орбиту а-углеродного атома вызывает у последнего возникновение отрицательного заряда и нуклеофильной реакционности, что затрудняет электрофильную реакцию с гидроксилом. [15]
Страницы: 1 2 3 4