Наличие - межмолекулярная сила
Cтраница 1
Наличие межмолекулярных сил и объема молекул приводит к отклонению свойств реальных газов от свойств идеальных газов. Вследствие различия молекулярных объемов и сил взаимодействия между разными молекулами свойства реальных растворов отличаются от свойств идеальных растворов. Поэтому с возрастанием плотности и давления газа и с понижением температуры увеличивается различие между свойствами реальных и идеальных газов; с ростом давления и с увеличением различия в химическом составе и физических свойствах компонентов раствора отклонение свойств реальных растворов от свойств идеальных растворов также увеличивается. [1]
Наличие межмолекулярных сил мало сказывается на подвижности молекул в газовой фазе. В кристаллах взаимодействие между молекулами или ионами выражено сильно, поэтому образуются жесткие структуры. В жидкостях кинетическая энергия молекул сравнима с потенциальной энергией их взаимодействия. [2]
Наличие межмолекулярных сил отталкивания приводит к тому, что молекулы могут сближаться между собой только до некоторого минимального расстояния. Поэтому можно считать, что свободный для движения молекул объем будет равен v - Ь, где Ъ - тот наименьший объем, до которого можно сжать газ. [3]
Ввиду наличия значительных межмолекулярных сил взаимодействия, асфальтены проявляют свойства вьгсокоэластичности. [4]
Действительно, при наличии межмолекулярных сил, внутренняя энергия слагается не только из кинетической энергии теплового движения, но и из потенциальной энергии, зависящей от взаимного расположения молекул. Нетрудно видеть, что доля потенциальной энергии, которая связана с силами отталкивания, убывает при взаимном удалении молекул, а доля, связанная с наличием сил притяжения, - возрастает. Понятно, поэтому, что должно иметься такое расстояние между молекулами, на котором суммарная потенциальная энергия будет иметь минимум. Это расстояние соответствует положению устойчивого равновесия. [5]
Де-Бройн [6,153, 154] и другие исследователи [155] приходят к выводу, что смачивание является необходимым условием хорошей адгезии, так как оно указывает на наличие сильных межмолекулярных сил на поверхности, приводящих к межмолекулярному взаимодействию адгезива и субстрата. [6]
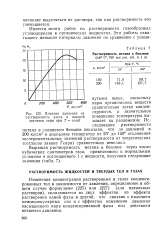 |
Влияние давления на. [7] |
Изменение концентрации растворенных в газах конденсированных тел в зависимости от давления, определяемое в общем случае формулами ( 225) или ( 227) ( для идеальных растворов), складывается из двух эффектов: из эффекта растворения одной фазы в другой, что связано с наличием межмолекулярных сил и с эффектом изменения давления насыщенного пара конденсированной фазы под действием внешнего давления. [8]
Исходя из наличия межмолекулярных сил, видно, что это поведение отражает условие, при котором межмолекулярные расстояния настолько уменьшились, что взаимно отталкивающие силы оказывают чрезвычайное сопротивление дальнейшему уменьшению объема. [9]
Межмолекулярное взаимодействие влияет прежде всего на кинетическое поведение макромолекул. Так, наличие межмолекулярных сил определяет стеклование полимеров в блоке. Для высокоэластической деформации необходимо наличие гибкости у полимерных цепей. Поэтому при тех температурах, при которых межмолекулярные силы способны фиксировать положение звеньев макромолекул в блоке, высокоэластическая деформация невозможна и полимер находится в стеклообразном состоянии. Соответствующие представления были развиты / Курковым [37] при построении теории пластификации полимеров. [10]
Тот экспериментальный факт, что газовые смеси представляют собой растворы, позволяет рассматривать вопросы растворимости газов в газах или ограниченной взаимной растворимости газов при температурах выше критической температуры обоих компонентов. Значительная плотность сжатых газов и наличие больших межмолекулярных сил объясняет возможность расслоения в таких растворах. [11]
Слово вириалъный происходит от латинского vis ( множественное число vires), означающего сила. Вириальные коэффициенты определяют отклонение от идеальности вследствие наличия межмолекулярных сил. [12]
Итак, несмотря на малый радиус действия молекулярных сил между двумя частицами, роль этих сил возрастает, когда во взаимодействие вступают конденсированные тела. Теоретические расчеты и прямые эксперименты, подтвердившие наличие значительных межмолекулярных сил, сравнительно медленно убывающих с расстоянием, играют огромную роль в понимании механизма многих поверхностных явлений, в том числе и адгезии. Имеются многочисленные свидетельства того, что молекулярное поле твердой поверхности не ограничивается расстоянием в несколько ангстремов, а простирается значительно дальше. Поэтому есть все основания говорить о трехмерных аспектах поверхностных явлений [33], о влиянии твердой поверхности на структуру и свойства прилегающих слоев второй фазы и других проявлениях пристенного эффекта, вызванного дальнодействием поверхностных молекулярных сил. Несомненно, немалую роль эти эффекты играют и при адгезии. III будет подробно рассмотрен вопрос о влиянии твердой поверхности на структуру и свойства прилегающих слоев. Здесь мы ограничимся некоторыми примерами, наиболее ярко иллюстрирующими эффекты дальнодействия, и отметим, что в случае полимерных адгезивов и покрытий они проявляются особенно четко благодаря особенностям структуры этих материалов - наличию крупных надмолекулярных образований. [13]
При понижении температуры межмолекулярное взаимодействие приводит к образованию жидкости. Это эквивалентно появлению некоторого внутреннего давления П, вызванного наличием межмолекулярных сил. [14]
Ориентация и межмолекулярные силы При вытяжке полиамидные смолы легко ориентируются; при этом между атомами кислорода карбонильных групп и водородными атомами, связанными с азотом аминогрупп соседних молекул, возникают весьма прочные межмолекулярные врдородные связи. Межмолекулярные силы оказывают значительное влияние на температуру плавления, прочность волокна и растворимость; наличие прочных межмолекулярных сил обусловливает ценные технические свойства полимера. [15]
Страницы: 1 2