Наличие - сильное взаимодействие
Cтраница 1
Наличие сильного взаимодействия между молекулами в твердом - кристаллическом или аморфном - состоянии вещества, сохраняющего существенную роль в жидком состоянии, придает их макроскопическим свойствам большее разнообразие, чем в случае газообразного состояния. [1]
Наличие сильного взаимодействия ал. [2]
При наличии сильного взаимодействия такого рода, молекулы жидкости, расположенные вокруг коллоидных частиц, как бы скрепляются и лишаются своей подвижности. Благодаря такому взаимодействию поверхностный слой приобретает несколько упорядоченную и уплотненную структуру. Это явление, в известной мере, подобно адсорб-ции ( см. гл. Вследствие этого частицы переме-вдаются совместно с прилежащим к их поверхности, слоем, , жидкости и при сближении двух частиц они как бы упи - раются друг в друга скрепленными с ними слоями жидкости. Для полного сближения частиц необходимо растолкать теснящиеся к ним молекулы. [3]
При наличии очень сильного взаимодействия между разноименными атомами критическая температура Тс, при которой происходит разупорядочение, может оказаться выше температуры плавления материала. Такие сплавы имеют сходство с химическими соединениями ( см. гл. Если взаимодействие между разнородными атомами является менее интенсивным, то упорядоченный твердый раствор может стать разупорядоченным при некоторой критической температуре, даже если его состав отвечает строго определенному стехиометрическому соотношению, подобному формуле соединения. Такое явление наблюдается для многих типичных фаз в металлических сплавах при повышении температуры. Наконец, если упорядочивающие силы очень незначительны, как, например, в области малых концентраций при образовании ограниченных твердых растворов, то критическая температура может лежать ниже температуры, при которой возможно достижение равновесия в приемлемых пределах времейи. В таком случае можно сказать, что разупорядоченное состояние является замороженным. [4]
При наличии очень сильного взаимодействия между разноименными атомами критическая температура Тс, при которой происходит разупорядочение, может оказаться выше температуры плавления материала. Такие сплавы имеют сходство с химическими соединениями ( см. гл. Если взаимодействие между разнородными атомами является менее интенсивным, то упорядоченный твердый раствор может стать разупорядоченным при некоторой критической температуре, даже если его состав отвечает строго определенному стехиометрическому соотношению, подобному формуле соединения. Такое явление наблюдается для многих типичных фаз в металлических сплавах при повышении температуры. Наконец, если упорядочивающие силы очень незначительны, как, например, в области малых концентраций при образовании ограниченных твердых растворов, то критическая температура может лежать ниже температуры, при которой возможно достижение равновесия в приемлемых пределах времени. В таком случае можно сказать, что разупорядоченное состояние является замороженным. [5]
Кроме того, наличие сильного взаимодействия между нуклонами приводит к тому, что коллективные и одночастичные состояния не всегда удается четко разделить. Первоначально считалось, что при наличии столь сильного взаимодействия говорить о заполнении одночастичных состояний в ядрах вообще не имеет смысла. Напомним, однако, что основной причиной существования подобных состояний как в ядрах, так и в атомах, молекулах и кристаллах, является вовсе не интенсивность взаимодействия, а регулирующая роль принципа Паули. Если какие-то состояния в соответствии с принципом Паули заполнены, то находящиеся в них частицы не могут взаимодействовать независимо от того, велика или нет интенсивность взаимодействия. [6]
Типы А и В характеризуются наличием сильного взаимодействия между солюбилизованными веществами и мицеллами ПАВ, что выражается в крутом наклоне касательной к изотерме сопюбилизащш при малых концентрациях ПАВ. Далее для типа А характерно плато при умеренных концентрациях, указывающее на образование комплекса. [7]
Это заставляет сделать вывод о наличии сильного взаимодействия между обоими партнерами, образующими комплекс, причем в свете сказанного выше зто взаимодействие не может быть в заметной степени электростатическим. Кроме того, известно, что эти комплексы часто бывают окрашены; так, например, окрашены растворы ароматических соединений в безводном фтористом водороде или в серной кислоте. Комплексы с иодом дают в УФ-спектре наряду с полосами поглощения компонентов новые полосы в области 300 ммк, относящиеся к комплексу. С другой стороны, об истинном химическом соединении речь не может идти, так как ненасыщенные соединения могут быть вновь выделены из их комплексов в неизмененном виде при разбавлении раствора водой. При этом не происходит даже изомеризации склонных к перегруппировке соединений. Например, комплексообразование с D2SO4 протекает без дей-терообмена. [8]
Растворение солей в ацетоне всегда связано с наличием сильного взаимодействия между растворителем и растворенным веществом; из таких растворов могут быть выделены твердые соединения. [9]
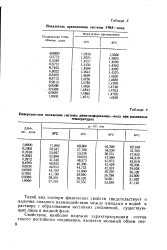 |
Показатель преломления системы ГМА-вода. [10] |
Такой вид изотерм физических свойств свидетельствует о наличии сильного взаимодействия между амидами и водой в растворе с образованием нестойких соединений, существующих лишь в жидкой фазе. [11]
Следует различать два предельных случая: первый характеризуется наличием сильного взаимодействия кристаллов, когда силы, возникающие на поверхности раздела между двумя слоями атомов различных веществ, по величине больше сил взаимодействия между двумя слоями одного кристалла; второй случай соответствует слабому взаимодействию между слоями различных веществ по сравнению с взаимодействием в пределах одного кристалла. [12]
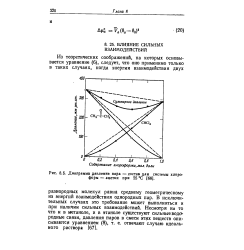 |
Диаграмма давление пара - состав для системы хлороформ - ацетон при 25 С 168 ]. [13] |
В исключительных случаях это требование может выполняться и при наличии сильных взаимодействий. [14]
Как давно известно, свойства некоторых жидкостей и растворов указывают на наличие необычно сильного взаимодействия между молекулами растворителя, или между молекулами растворителя и растворенного вещества, или же между митекула-ми самого растворенного вещества. Вместо температуры плавления - 100 С, как это можно было бы ожидать при экстраполяции температур плавления Н2Те, H2Se и H2S, вода плавится при 0 С. [15]
Страницы: 1 2 3 4