Наложение - катодный ток
Cтраница 1
Наложение катодного тока приводит к быстрой поляризации титановых катодов. Однако участки кривых, отвечающие выделению водорода, для всех трех кислот расположены сравнительно невысоко - очевидно титан является достаточно эффективным катодом при водородной деполяризации. [1]
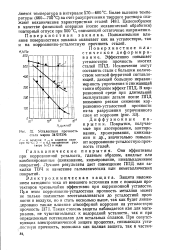 |
Усталостная прочность стали марки 34ХНЗМ. [2] |
Защита наложением катодного тока от внешнего источника или с помощью протекторов чрезвычайно эффективно при коррозионной усталости. Такая степень защиты наблюдается как для материалов, не чувствительных к водородной усталости, так и при определенных потенциалах для остальных сплавов. [3]
При наложении катодного тока сплошность покрытия образцов нарушается раньше на образцах с более отрицательными значениями потенциалов. [4]
 |
Схема перехода водорода с поляризационной стороны мембраны на диффузионную. [5] |
При наложении катодного тока на поляризационную сторону мембраны и смещении ее потенциала в отрицательном направлении выделение водорода вначале происходит только на поляризационной стороне, а затем и на диффузионной. [6]
Установлено, что наложение катодного тока при малых коэффициентах интенсивности напряжений К / замедляет скорость развития трещин, а при больших К / ускоряет ее. [7]
Кривые заряжения могут сниматься при наложении анодного и катодного тока. Этот метод исключает длительное протекание электрохимического процесса на исследуемом электроде при постоянном потенциале, так как последний непрерывно меняется в зависимости от количества пропущенного электричества. [8]
Эти данные позволяют установить, что защитному эффекту при наложении катодного тока предшествует некоторое ускорение растрескивания. [9]
Начальные значения потенциала этой стали в неаэрируемых растворах имеют более отрицательные значения и при наложении катодного тока также приближаются к - 200 мв. [10]
Решающим фактором эффективности катодной защиты является электродный потенциал, который приобретает защищаемый объект при наложении катодного тока. Электродный потенциал измеряют по отношению к электроду сравнения, например при измерениях в воде - к хлоридсеребряному, а в почве - к медносульфатному электроду. Измеряемая величина должна быть исправлена на омическое падение потенциала, существующее между электродом сравнения и защищаемым объектом; для этого имеются специальные методы. [12]
Поэтому применение покрытий на их основе в условиях комплексной защиты нецелесообразно, так как при наложении катодного тока на изолированные стальные конструкции на границе металл-покрытие происходит накапливание щелочи в результате электролиза. [13]
Плотность анодного тока растворения ВС определяется путем измерения потерь веса образ ца, выдерживаемого при постоянном потенциале, посредством наложения катодного тока плотностью CD. Для каждой точки требуется отдельный образец. [14]
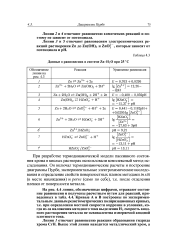 |
Данные о равновесиях в системе Zn - H2O при 25 С. [15] |
Страницы: 1 2 3
