Наложение - катодный ток
Cтраница 2
На рис. 4.4 линии, обозначенные цифрами, отражают состояние равновесия и получены расчетным путем для реакций, приведенных в табл. 4.4. Кривые А и В построены по экспериментальным данным резистометрических поляризационных кривых, т.е. при определении местной скорости коррозии в условиях, когда из-за наложения катодного тока выделения Н2 скорость анодного растворения металла не эквивалентна измеряемой анодной плотности тока. [16]
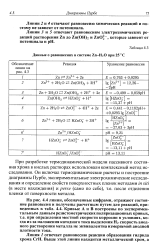 |
Данные о равновесиях в системе Zn - H2O при 25 С. [17] |
На рис. 4.4 линии, обозначенные Цифрами, отражают состояние равновесия и получены расчетным путем для реакций, приведенных в табл. 4.4. Кривые А и В построены по экспериментальным данным резистометрических поляризационных кривых, т.е. при определении местной скорости коррозии в условиях, когда из-за наложения катодного тока выделения ЬЬ скорость анодного растворения металла не эквивалентна измеряемой анодной плотности тока. [18]
 |
Данные о равновесиях в системе Zn-F O при 25 С. [19] |
На рис. 4.4 линии, обозначенные цифрами, отражают состояние равновесия и получены расчетным путем для реакций, приведенных в табл. 4.4. Кривые А и В построены по экспериментальным данным резистометрических поляризационных кривых, т.е. при определении местной скорости коррозии в условиях, когда из-за наложения катодного тока выделения Нз скорость анодного растворения металла не эквивалентна измеряемой анодной плотности тока. [20]
Без поляризации электрода катализатора ( кривая 1) процесс идет с постоянной скоростью до конца реакции. Наложение катодного тока на электрод-катализатор ( кривые 2, 3 к 4) различным образом отражается на кинетике гидрирования двойной и тройной связи: на кинетической кривой появляется ясно выраженный максимум, после которого скорость поглощения водородом из газовой фазы резко снижается, сохраняя затем постоянное значение до конца опыта. Анализ реакционной смеси свидетельствует о том, что процесс электрокаталитического гидрирования диметилэтинилкарбинола идет селективно, причем при максимальной скорости происходит гидрирование диметилэтинилкарбинола до диметилвинилкарбинола, который по мере образования вытесняется исходным веществом с поверхности катализатора в раствор. На участке кинетической кривой, отличающемся постоянной скоростью поглощения водорода, гидрируется двойная связь. Характерно то, что, как и в случае гидрирования хинона, при электрокаталитическом гидрировании диметилэтинилкарбинола ( плотность тока 4 - 10 - 4 а / см2) скорость поглощения первого моля водорода из газовой фазы больше, чем скорость гидрирования ацетиленовой связи без поляризации. Кинетика гидрирования двойной связи диметилвинилкарбинола напоминает кинетику электрокаталитического гидрирования малеиновой кислоты, а именно, с наложением тока поляризации скорость поглощения водорода из газовой фазы резко уменьшается. [21]
В сплаве имеется недостаток компонента А и избыток компонента В. При наложении катодного тока баланс скоростей реакции нарушается - - происходит ускорение внедрения металла. [22]
 |
Химический состав эмали и водной вытяжки из нее.| Зависимость прочности сцепления от содержания в грунтовой эмали окиси кобальта. [23] |
При качественном нанесении эмалевые покрытия обеспечивают высокую степень защиты в условиях, когда на стальную конструкцию не действует электрический ток. В результате наложения постоянного катодного тока довольно быстро разрушается эмалевое покрытие, которое отслаивается в виде вытянутых чешуек; при действии анодного тока происходит локализованное сквозное проржавление. [24]
Поэтому на практике вопрос выбора ингибитора должен быть тщательно продуман, иначе может иметь место повышение абсорбции водорода. Травление при наложении катодного тока способствует чрезмерно большой абсорбции водорода и поэтому применять его не следует, но анодное травление или травление в окислительных кислотах могут быть использованы при принятых мерах предосторожности. [25]
ОН - к ионам хлора, то в титане трещины при коррозионном растрескивании не распространяются. Катодная защита в нейтральных или в слабо кислых растворах может быть объяснена образованием сильнощелочного раствора в результате общего расхода ионов водорода. В сильнокислых растворах при наложении катодного тока электролит в трещине не может становиться щелочным. Поскольку в вершине трещины поддерживается компромиссный потенциал, наложение катодного тока не должно приостановить растрескивание в очень кислых растворах. [26]
При катодной поляризации металла от внешнего источника тока у его поверхности происходит непрерывное образование щелочи. Если испытание проводится в непроточном растворе, то поляризация с течением времени смещает значение рН раствора в щелочную область. Так, по данным работы [18] при наложении катодного тока плотностью 5 мА / см2 ( необходимого для полной защиты стали от коррозионной усталости в 3 % - ном растворе NaCl) у поверхности в 1 дм2 каждую минуту образуется 31 3 мг едкого натра. Поэтому некоторое увеличение долговечности образцов из алюминиевого сплава АМгЗ, имевшее место при плотностях катодного тока до 1 мА / см2, объяснено именно небольшим повышением щелочности раствора, благоприятствующим, по мнению авторов, упрочнению защитной пленки на алюминиевом сплаве. [27]
По результатам наших испытаний [8], в насыщенном водном растворе сероводорода, а также IB растворе роданистого аммония при комнатной температуре напряженная термически упрочненная арматура подвергалась быстрому хрупкому разрушению. Высокопрочная холоднотянутая проволока оказалась значительно более стойкой. Разрушение напряженных образцов в растворе сероводорода происходило ви зрительно быстрее при наложении катодного тока, что характерно для ( водородного охрупчивания. [28]
На рис. 4.15 представлена кривая заряжения для стали 06ХН28МДТ в промышленном перемешиваемом растворе гидр-оксиламинсульфата. Параллельно измеряли емкость двойного электрического слоя. Точки на кривой ABCZDEK соответствуют значениям потенциала в конце пауз между импульсами тока, точки на кривой MNOPS - значениям потенциала в моменты наложения катодного тока. После активации образца при ф - 0 7 В в течение 3 мин устанавливается потенциал ф - 0 32 В. Вначале потенциал медленно сдвигается в область положительных значений ( участок АВ), а через 1 - 1 5 ч происходит пассивация поверхности фст 0 23 В. Участок N0 свидетельствует о сдвиге потенциала от стационарного во времени. Сдвиг потенциала при поляризации достигает максимума ( ОР), затем поверхность активируется и цикл повторяется. [29]
Палладий по своему поведению при электрохимическом выделении водорода во многом похож на платину. Опытные данные по величинам токов обмена и наклону тафелевских прямых указывают на заторможенность рекомбинации как на вероятную причину водородного перенапряжения. Кобозев и Монбланова ( 1935) доказали медленное протекание стадии рекомбинации на электродах из палладия. При наложении катодного тока на поляризационную сторону мембраны и смещении ее потенциала в отрицательном направлении выделение водорода вначале происходит только на поляризационной стороне, а затем и на диффузионной. [30]
Страницы: 1 2 3