Некарбонатная жесткость - вода
Cтраница 2
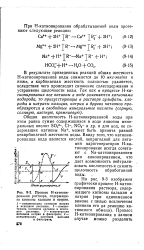 |
Процесс Н - катионирования раствора, содержащего катионы кальция и натрия. [16] |
Общая кислотность Н - катионированной воды при этом равна сумме содержащихся в воде анионов минеральных кислот SC42 -, Cl -, NO3 - и др. и для вод, не содержащих катионы Na, может быть принята равной некарбонатной жесткости воды. Ввиду того, что катиони-рованная вода является кислой, непригодной для питания парогенераторов Н - ка-тионирование всегда сочетают с Na-катионированием или анионированием, что дает возможность нейтрализовать кислотность и снизить щелочность обработанной воды. [17]
Присутствие сульфатов в природных водах обусловлено выветриванием пород и биохимическими процессами в водоносных слоях. Их содержание обусловливает некарбонатную жесткость воды. [18]
Естественное содержание-сульфатов в поверхностных и грунтовых водах обусловлено выветриванием пород и биохимическими процессами в водоносных слоях. Их содержание определяет в известной мере некарбонатную жесткость воды. Содержание сульфатов в водоемах может быть повышенным вследствие сброса в них сточных. [19]
Естественное содержание сульфатов в поверхностных и грунтовых водах обусловлено выветриванием пород и биохимическими процессами в водоносных слоях. Их содержание определяет в известной мере некарбонатную жесткость воды. Содержание сульфатов в водоемах может быть повышенным вследствие сброса в них сточных вод с неорганическими и органическими соединениями серы. [20]
Если карбонатная жесткость приблизительно равна некарбонатной, соду можно совсем не добавлять, так как необходимое количество ее для умягчения такой воды образуется в результате реакции бикарбонатов с NaOH. Доза кальцинированной соды увеличивается по мере повышения некарбонатной жесткости воды. Содонатровый метод обычно применяется для умягчения вод, в которых карбонатная жесткость немного больше некарбонатной. [21]
Одновременно гидроокись алюминия реагирует с карбонатами, растворенными в воде. Вследствие этого кроме осветления воды достигается уменьшение ее карбонатной жесткости и одновременно увеличивается некарбонатная жесткость воды. [22]
При этом в фильтрате снижаются кальциевая жесткость и бикарбонат - ная щелочность, возрастают карбонатная щелочность и магниевая жесткость. Возможно также непосредственное растворение таких составляющих сорбента, как MgCh и СаСЬ, что сцпровождается возрастанием некарбонатной жесткости воды. При таких условиях работы первоначально достигается высокий эффект обескремнивания, но при этом, взаимодействуя с НСОТ и СО2, сорбент интенсивно разрушается. Сопротивление фильтров прогрессивно растет и не устраняется полностью при их взрыхлении, затем эффект удаления кремнекислых соединений резко падает. Поэтому обескремнивание на сорбенте сырой или коагулированной воды нецелесообразно. [23]
От концентрации отдельных солей зависит пригодность воды для оборота. Основными солями стока, который подвергался исследованию, были хлориды, сульфаты, карбонаты Na -, Ca-2, Fe-3 и др. Наличие сульфатов в воде в большом количестве нежелательно, так как сульфаты кальция и магния повышают некарбонатную жесткость воды. [24]
Разложение бикарбоната магния протекает по аналогичному уравнению. Образующиеся карбонаты кальция и магния нерастворимы в воде и выпадают в осадок, причем жесткость воды, обусловленная бикарбонатами указанных металлов, устраняется. Кипячением некарбонатная жесткость воды не устраняется. [25]
Разложение бикарбоната магния протекает по аналогичному уравнению. Образующиеся карбонаты кальция и магния нерастворимы в воде и выпадают в осадок, причем жесткость воды, обусловленная бикарбонатами указанных металлов, устраняется. Путем кипячения некарбонатная жесткость воды не устраняется. [26]
В объемном анализе часто прибегают к способу обратного титрования остатка. Этот способ используют при определении некарбонатной жесткости воды, при определении аммиака, при определении гумуса в почве, при определении азота в органических веществах и во многих других случаях, когда непосредственное титрование определенного вещества затруднительно. Прием состоит в том, что к определяемому веществу прибавляют точно измеренный избыток раствора вещества известной концентрации, реагирующий с определяемым веществом. Затем остаток прибавленного реактива титруют раствором другого реактива с известной концентрацией. [27]
Естественное содержание сульфатов в поверхностных и грунтовых водах обусловлено выветриванием пород и биохимическими процессами в водоносных слоях. Повышенная концентрация сульфатов может свидетельствовать о загрязнении источника сточными водами, в основном производственными. В известной степени содержание сульфатов определяет некарбонатную жесткость воды. [28]
Поэтому данный метод применяется лишь с учетом соотношений между карбонатной и некарбонатной жесткостью. Если карбонатная жесткость приблизительно равна некарбонатной, соду можно совсем не добавлять, так как необходимое количество ее для умягчения такой воды образуется в результате реакции бикарбонатов с NaOH. Доза кальцинированной соды увеличивается по мере повышения некарбонатной жесткости воды. [29]
Содово-натриевый метод обычно применяют для умягчения воды, карбонатная жесткость которой немного больше некарбонатной. Если карбонатная жесткость приблизительно равна некарбонатной, соду можно совсем не добавлять, поскольку необходимое ее количество для умягчения такой воды образуется в результате взаимодействия гидрокарбонатов с едким натром. Доза кальцинированной соды увеличивается по мере повышения некарбонатной жесткости воды. [30]
Страницы: 1 2 3