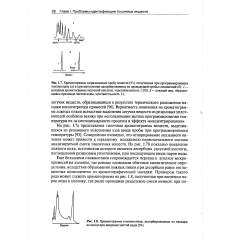
Хроматографическая насадка
Cтраница 1
Хроматографические насадки с химически связанными силиконовыми фазами обеспечивают превосходную эффективность и стабильность колонки, снижают вероятность потери распределительной фазы из носителя в процессе работы со стандартными жидко-жидкостными хроматографическими колонками. Кроме того, сильнополярные подвижные фазы, например хлороформ и водно-спиртовые смеси, могут быть использованы для быстрого вымывания сильно удерживаемых компонентов образца без заметного изменения свойств хроматографических колонок. Целесообразность использования в стандартной ЖЖХ этой сильнополярной подвижной фазы весьма сомнительна из-за ее высокой растворяющей способности по отношению к неподвижным фазам. [1]
Хроматографическую насадку ( 3 % OV-1 на хроматоне N-AW) готовят следующим образом: в колбу с притертой пробкой вносят 1 5 г OV-1, заливают 50 - 100 см3 хлороформа, закрывают пробкой и оставляют на сутки для набухания. В стеклянный стакан помещают 50 г твердого носителя хроматон N-AW фракции 0 20 - 0 25 мм и приливают к нему приготовленный раствор OV-1 в хлороформе. Растворитель удаляют при нагревании на водяной бане и при перемешивании. [2]
Для приготовления хроматографической насадки ( 15 % полифенилового эфира 5Ф - 4Э и 1 % НзРО4 ( масс.) на хроматоне N-Супер) рассчитанное количество эфира и ортофос-форной кислоты растворяют в хлороформе и полученным раствором в фарфоровой чашке обрабатывают твердый носитель обычным способом. Хроматографиче-скую колонку заполняют сорбентом с помощью вакуумного водоструйного насоса и закрывают ее концы тампонами из стекловолокна. Готовую колонку помещают в термостат хроматографа и, не подключая ее к детектору, кондиционируют сорбент в токе газа-носителя ( азот или гелий) при расходе около 50 см3 / мин в течение 8 ч при температуре 140 С. После этого колонку присоединяют к детектору. [3]
Стеклянную колонку, заполненную хроматографической насадкой кондиционируют в токе газа-носителя постепенно повышая температуру испарителя до 350 С в течение 8 - 10 часов, а затем подключают к детектору и выводят на рабочий режим. [4]
 |
Схема устройства для адсорбционного концентрирования. [5] |
В качестве сорбентов для концентрирования постоянных газов и легких углеводородов используют молекулярные сита, силикагель, активный уголь и др. При анализе более высококипящих веществ - хроматографические насадки ( твердый носитель с неподвижной фазой) и пористые полимерные сорбенты, например тенакс. [6]
Еще большими сложностями сопровождается переход к анализу микропримесей на колонке, где раньше проводили обычные аналитические определения, вследствие образования ложных пиков при десорбции ранее поглощенных компонентов из хроматографической насадки. [8]
Реакционная хроматография относится к тем немногим вариантам анализа, которые позволяют надежно идентифицировать и определять высокополярные алканоламины ( аминоспирты), микропримеси которых при прямом хроматогра-фировании необратимо сорбируются хроматографической насадкой и некоторыми частями аппаратуры. Загрязненный воздух пропускают через ловушку с А12О3 и десорбируют сконцентрированные примеси водным раствором октансульфокислоты. [9]
 |
Хроматограмма водорода. i 1. [10] |
Помимо водорода при пиролизе органических соединений часто образуются газы: кислород, азот, метан, моноксид и диоксид углерода. Не известно ни одной хроматографической насадки, которая могла бы обеспечить разделение всех газов этой группы, а тем более в смеси с водородом при какой-либо одной температуре колонки. [11]
Таким способом можно успешно приготовить колонки с хроматографической насадкой типа пермафаза. Тем не менее условия для суспензионного способа заполнения колонок изучены недостаточно, чтобы оптимизировать методику. Результаты иногда отличаются по причинам, которые не были установлены. [12]
Другой путь заключается в детальном исследовании процессов, приводящих к аномальному поведению уже известных летучих хелатов металлов в колонках, и в поиске способов устранения нежелательных эффектов. Результатом исследований в этом направлении может быть появление новых хроматографических насадок, исключающих сорбцию хелатов и химическое взаимодействие с ними, а также дальнейшее развитие методов газовой хроматографии с модифицированной подвижной фазой и разработка других специальных вариантов газовой хроматографии. [13]
Не менее важной является надежная идентификация хлорфенолов, которые могут служить потенциальным источником таких супертоксикантов, как ПХБ и диоксины. Кроме того, прямой анализ хлорфенолов затруднен, так как они являются сильными кислотами и могут сорбироваться хроматографическими насадками. [14]
Как загрязнитель воздуха гидразин часто сопутствует аммиаку и другим азотсодержащим неорганическим газам и ЛОС. Прямое определение N2H4 ( обычно в смеси с алкилгидразинами) затруднено, поскольку он взаимодействует со многими хроматографическими насадками. Существует и проблема извлечения гидразина из воздуха, также связанная с его реакционной способностью и невозможностью использовать для его улавливания традиционные сорбенты. [15]
Страницы: 1 2