Бейтман
Cтраница 1
Бейтман [60] подчеркивает предпочтительность более общего определения неполной гамма-функции через вырожденную гипергеометрическую функцию. [1]
Бейтман и др. [30] показали, что замещение хлора в бенз-гидрилхлориде нуклеофильными реагентами - ионом фтора, пиридином или триэтиламином в жидкой двуокиси серы - имеет одинаковую начальную скорость, не зависящую от природы ну-клеофила. [2]
Бейтман, Мур и Портер3 доказали большим количеством экспериментальных данных, что реакция вулканизации должна иметь ионный характер. [3]
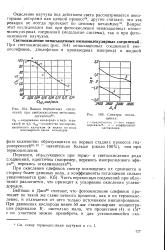 |
Выход перекисных соединений при светоокислении метилцик. [4] |
Бейтман и Джи38 считают, что фотоокисление олефинов протекает по такой же схеме цепного процесса, как и их термоокисление, и отличается от него только источником инициирования. [5]
Бейтман и Хьюз [1] показали, что при растворении трет-бутилхлорида в безводной муравьиной кислоте между трет-бу-тилхлоридом, ионами хлора и изобутиленом быстро устанавливается равновесие. [6]
Теорема Бейтмана, согласно которой уравнения Максвелла инвариантны относительно конформных преобразований ( § 28), содержится в этом положении как частный случай. [7]
Изучение Бейтманом с сотрудниками27 аутоокнсленпя предельных и непредельных сульфидов показало, что продуктами этой реакции являются главным образом сульфоксиды и продукты распада. Они считали, что при этом происходит образование промежуточных перекисей или перокси-радикалов: по-видимому, сульфидная группа аналогично функциональной группе простого эфира, активирует соседние метиленовые С - Н - связи. [8]
Обнаруженное Бейтманом перемещение двойных связей в процессе серной вулканизации НК можно также рассматривать и как указание на промежуточное образование сво бодных радикалов в полимерной цепи. Степень превращения определяется длительностью существования свободного радикала, которая зависит от состава вулканизующей системы и количества таких ингредиентов, как жирные кислоты и их мыла, прежде всего из-за гетерогенного характера реакции. Действительно, чем более выражен гетерогенный характер реакции, тем больше вероятность реакции в клетке, а следовательно, меньше время жизни полимерного радикала и степень перемещения двойных связей. [9]
Шелтон [2] и Бейтман [3] указали на большое влияние радикалов, образующихся при разложении перекиси, на скорость окисления полимеров. Окисление низкомолекулярного углеводорода, не содержащего перекисей, происходит автокаталитически и изображается кривой, аналогичной кривой 1 на рис. XIII-9. Анализ содержания перекисей при прогрессирующем окислении показывает, что в начальной стадии происходит накопление перекисей, приближающееся к максимуму, когда окисление достигает автокаталитической стадии. Распад перекисей, очевидно, в результате автокаталитической реакции происходит с большой скоростью, и концентрация перекиси уменьшается до очень небольшой постоянной величины. Вероятно, одновременное образование и распад перекисей в течение всей реакции окисления происходят с конкурирующими скоростями. По-видимому, радикалы, образующиеся в результате быстрого распада перекисей, обусловливают увеличение скорости окисления ( автокатализ), и эту стадию реакции обычно относят к реакциям разветвления цепей. При окислении полимеров инициирование, вероятно, в основном обусловлено радикалами, образующимися при распаде перекиси. Эти радикалы реагируют и с ингибиторами НА, дезактивируя их. Таким образом, эффективная стабилизация происходит в том случае, когда устраняется возможность распада перекиси на радикалы. [10]
По данным Барнарда и Бейтмана [3] окисление насыщенных диалкил -, арилалкил - и диарилсульфидов без катализаторов не происходит. В присутствии некоторых катализаторов, например азоизобутиронитрила, насыщенные диалкил - и арилалкилсульфиды окисляют до соответствующих сульф-оксидов. Реакция протекает по свободно-радикальному механизму и приводит к образованию большого количества побочных продуктов. Образующиеся при окислении сульфоксиды сильно тормозят протекание реакции. [11]
Это соотношение, как показал Бейтман [76] для ряда углеводородов, хорошо описывает зависимость w от [ ROOH ] в очень широком диапазоне концентраций гидроперекиси. [12]
Рассмотрим в этой связи данные Бейтмана [ 3, с. [13]
Такого рода эффект рассмотрен в работе Бейтмана и Хьюза. [14]
Сравните полученный вами результат с решением Бейтмана для этого случая при N и 7V §, не равных нулю. [15]
Страницы: 1 2