Белок - печень
Cтраница 1
 |
Пути превращения аминокислот в печени. [1] |
Белки печени подвергаются постоянному обновлению, причем для них характерна очень высокая скорость оборота со средним периодом полужизни всего лишь в несколько дней. Кроме того, именно в печени синтезируется большинство белков плазмы крови. [2]
Процесс обновления фосфора в фосфорсодержащих группировках белка печени происходит во много раз медленнее, чем в фосфолипидах. [3]
Как видно, нельзя сомневаться, что белки печени и других тканей обладают в условиях постоянства состава такой же скоростью кругооборота, устанавливаемой с помощью меченого фосфата, какая найдена с N16, Н3 и с радиоактивной серой - S33 ( гл. [4]
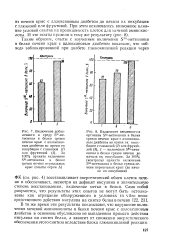
В период белкового голодания в первую очередь расходуются белки печени, а затем белки сыворотки крови. [5]
В период белкового голодания в первую очередь расходуются белки печени, а затем белки сыворотки крови. Но, принимая во внимание общий вес мускулатуры и кожи, можно считать, что около 2 / 3 потерь белка при общем голодании падает на их долю. [6]
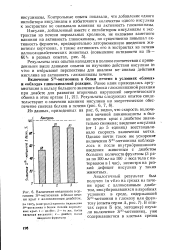 |
Включение введенного в организм 535-метионина в белки пече -, ни крыс с аллоксановым диабетом. [7] |
За 100 % ( контроль) принято включение 3 5-метионина в белки печени нормальных крыс. [8]
С-гуанидоаргинина и L - ( 3 - 3H) глутаминовой кислоты как в белки печени, так и в белки мышц. При этом авторы считают, что изменения темпов синтеза и деградации белков связаны с изменением интенсивности реутилизации аминокислот в организме, а не с изменением скоростей превращения их по обычным путям обмена. Реутилизация аминокислот, по их мнению, может быть сведена до минимума при обеспечении потребности животных в них за счет пищи. [9]
Признаками фиброзирующей реакции служили повышение скорости включения вводившегося в кровь меченого пролина ( аминокислота, входящая в состав коллагена) в белки печени, а при электронной микроскопии - отложения коллагена в перисинусои-дальные пространства Диссе. [10]
В качестве критериев состояния печени были избраны: синтез печенью мочевины и факторов свертывания крови ( протромбина, проконвертина и фактора V), содержание в печени жира, способность печени окислять тирозин и связывать фенолы, включение в белки печени меченного по сере радиоактивного метии-нина, содержание в сыворотке крови белка и белковых фракций. [11]
Многочисленные наблюдения больных в клиниках также свидетельствуют, что при голодании и тяжелых инфекционных заболеваниях, когда наблюдается интенсивный распад органов, в первую очередь снижается масса печени и мышц и существенно не изменяется масса мозга и сердца. Организм за счет распада белков печени и мышц обеспечивает нормальную деятельность жизненно важных органов. [12]
Аминокислоты либо используются для синтеза белков печени и плазмы, либо превращаются в глюкозу и гликоген в процессе глюконеогенеза. Аммиак, образующийся при дезаминировании аминокислот, включается в состав мочевины в ходе цикла мочевины. Жирные кислоты превращаются в печени в триацилглице-ролы, холестерол и лшюпротеины плазмы; последние обеспечивают транспорт и накопление липидов в жировой ткани. Кроме того, жирные кислоты в печени могут подвергаться окислению, что приводит к запасанию энергии в виде АТР и к образованию кетоновых тел, доставляемых кровью в другие ткани. [13]
В пользу этой точки зрения свидетельствуют как опыты на животных, так и исследования, проведенные на людях. В опытах на белых мышах было показано, что часть мескалина включается в клеточный белок печени и что время этого превращения соответствует сроку, в который развиваются психические нарушения у человека. Георги, Фишер и Вебер, применяя несколько модифицированную ими пробу Квика ( дополнительная нагрузка гликолом), нашли, что мескалин у большинства исследованных ими здоровых людей ведет к падению содержания в моче гиппуровой кислоты, тем более значительному, чем выше доза мескалина и чем отчетливее вызываемые им психические нарушения. Янтц, ссылаясь на изменения капилляров, обнаруженные у собак и морских свинок после введения мескалина, полагает, что через поврежденные мескали-ном капилляры выходит белок, что нарушает функцию клеток, главным образом печени и ведет к поступлению в кровь токсических веществ - промежуточных продуктов белкового обмена, которые и являются непосредственной причиной психоза Все эти данные слишком разрозненны и немногочисленны и не позволяют утверждать, что именно нарушение дезин-токсикационной функции печени или образование в печени какого-то нового вещества является причиной мескалинового психоза. Даже если принять гипотезу об образовании нового метаболита, то остается открытым вопрос о том, что это за метаболит. Наличие метоксильных групп в молекуле мескалина, очевидно, играет роль в возникновении галлюцинаций, так как р-фенилэтиламин не является галлюциногеном, но и тримето-ксифеиилуксусная кислота, в которой все метоксильные группы сохранены, также не оказывает токсического действия. Увеличение содержания МОФА при блокировании альдегиддегидрогеназы с помощью-карбамида кальция значительно усиливало токсическое действие мескалина, - отчетливые изменения поведения наступали быстрее и вызывались дозами, не оказывавшими в обычных условиях влияния на поведение животных. В то же время ипрониазид, замедляя окисление самого мескалина, не усиливал его токсического действия; не вызывал нарушений поведения и другой, образующийся из МОФА метаболит - триметоксифенил-этанол. Приводим схему обмена мескалина и его избирательного нарушения по Фридгоффу и Голдстейну. [14]
Страницы: 1 2