Пирофосфорнокислый натрий
Cтраница 3
Это разложение значительно замедляется в присутствии так называемых стабилизаторов, которыми чаще всего служат салициловая кислота или пирофосфорнокислый натрий, приливаемые в небольших количествах к раствору перекиси водорода. Однако при длительном хранении даже в присутствии стабилизаторов, перекись водорода медленно разлагается и содержание Н2О2 уменьшается. [31]
Перекись водорода, полученную неэлектрохимическим ( органическим) методом, стабилизируют ортофосфорной кислотой ( НзРО4) или пирофосфорнокислым натрием, подкисленным ортофосфорной или серной кислотой. [32]
Указывается, что покрытие таким сплавом, осаждаемое из ванны, содержащей цианистый цинк, едкий натр, хлористое олово и пирофосфорнокислый натрий, обладает хорошей защитной способностью, превышающей защитную способность кадмиевых покрытий. Приводятся [18] результаты исследования процесса совместного осаждения цинка и кобальта из сульфатноаммиачных растворов с получением сплавов с содержанием компонентов в широком интервале. [33]
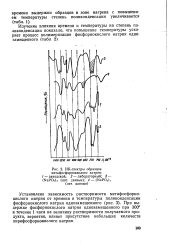 |
ИК-спектры образцов. [34] |
При выдержке фосфорнокислого натрия однозамещенного при 300 в течение 1 часа на величину растворимости получаемого продукта, вероятно, влияет присутствие небольших количеств пирофосфорнокислого натрия. [35]
Пирофосфатный электролит меднения содержит в основном комплексные пирофосфорнокислые соли меди MeCuP2O7, Me6Cu ( P2O7) 2 ( где Me - К или Na) и пирофосфорнокислый натрий Na4P2O7 или пирофосфорнокислый калий IC O. Так как растворимость в воде Na4P2O7 значительно меньше IC O. [36]
В колбасном производстве широко используют фосфат натрия, одно - ( Е339 ( 0), дву - ( ЕЗЗЭТЮ), трех - ( Е339 ( Ш)) и четырехзамещенный пирофосфорнокислый натрий. Эти соли обладают высоким свойством увеличивать влагосвязывающую способность колбасного фарша. Триполифосфат и тетра-натрийпирофосфат обладают наиболее влагос-вязывающей способностью. Указанные соединения не влияют на интенсивность окраски колбас, а при хранении колбасы имеют наименьшую потерю массы. [37]
Посуда и реактивы: 1) пипетка на 25 мл; 2) мерная колба на 250 мл; 3) коническая колба на 250 мл; 4) 10 / о-ный раствор пирофосфорнокислого натрия N34P207 10Н2О; 5) раствор H2SO4 ( 1: 4); 6) 20 / о-ный раствор сернокислого аммония ( NH4) 2SO4; 7) 1 % - ный раствор дифениламина в серной кислоте ( уд. [38]
Цианистый комплекс разрушают нагреванием с серной и азотной кислотами. Железо связывают в комплекс пирофосфорнокислым натрием. [39]
Цианистый комплекс разрушают нагреванием с серной и азотной кислотами. Железо связывают в комплекс пирофосфорнокислым натрием. [40]
По окончании разложения полученный раствор упаривают почти досуха, к влажным солям приливают 2 - 3 мл соляной кислоты ( 14) и после выдержки раствора в течение 2 - 3 мин разбавляют его водой до 20 - 30 мл. В стакан для титрования емкостью 300 мл вносят 20 г пирофосфорнокислого натрия или 125 мл фосфатного раствора ( 16), опускают электроды и мешалку, включают электродвигатель и регулируют обороты мешалки так, чтобы жидкость энергично перемешивалась. Раствор прибавляют струей, наблюдая за показаниями гальванометра. Когда стрелка гальванометра начинает заметно колебаться, перманганат добавляют по каплям до первого устойчивого увеличения показаний гальванометра. Заметив этот момент, добавляют еще каплю перманганата, вновь замечают показание прибора и так продолжают титрование, пока очередная добавленная капля не даст меньшего прироста показаний по сравнению с предыдущей. Это и служит признаком окончания титрования. Если скачок при титровании очень мал, то рекомендуется платиновый электрод прокалить на горелке. Параллельно проводят титрование реактивной пробы: ее приготовляют по ходу определения без растворения анализируемой навески. Полученный раствор оттитровывают, как описано выше. [41]
Ванна 2 - пирофосфорнокислая - предназначается взамен цианистых ванн. Перед меднением в згой ванне изделия рекомендуют анодно декапировать в 10 % - ном растворе пирофосфорнокислого натрия при комнатной температуре в течение 0 5 - 1 0 мин. [42]
Гамова) производится растворением уксуснокислой меди в теплой воде и добавлением в избытке заранее растворенного в теплой воде пирофосфорнокислого натрия до просветления раствора меди. Раствор становится темносиним, прозрачным. При помутнении следует добавлять пирофосфорнокислый натрий. Затем добавляются остальные компоненты, заранее растворенные в теплой воде. Сцепление осадка меди с основным металлом будет хорошее при подготовке поверхности электрохимической полировкой. [43]
Если приблизительное содержание марганца в исследуемом сплаве неизвестно, - необходимо произвести предварительное испытание. Для этой цели 0 138 г сплава растворяют при нагревании в 3 5 мл 83 % - ной фосфорной кислоты, прибавляют 1 г пирофосфорнокислого натрия и 13 мл мононадфосфорной кислоты, нагревают, затем охлаждают и титруют, как выше описано. Число миллилитров серноватистокислого натрия, помноженное на 4, дает процентное содержание марганца. В случае сплавов с большим содержанием марганца этот метод дает пониженные результаты, вследствие восстанавливающего действия содержащихся в сплавах углеродистых соединений; при содержании Мп ниже 10 / 0 получаемые результаты бывают часто повышенными, так как незначительные количества марганца недостаточно ускоряют разложение избыточной мононадфоо. Поэтому при выполнении окончательного анализа фосфорнокислый раствор исследуемого материяла разбавляют водой, при - бавляют надсернокислого аммония и кипячением разрушают его избыток. Образовавшиеся высшие окислы марганца восстанавливают перекисью водорода, избыток которой устраняют затем небольшим количеством соли Мора, и лишь после этого проводят реакцию с мононадфосфорной кислотой. [44]
Сернокислый никель в электролите определяют объемным диметилглиоксимовым методом. Цианистый комплекс предварительно разрушают нагреванием с серной кислотой. Железо окисляют азотной кислотой и связывают в комплекс фтористым или пирофосфорнокислым натрием. [45]
Страницы: 1 2 3 4