Нахождение - точка - эквивалентность
Cтраница 2
Некоторые другие методы нахождения точки эквивалентности описаны в гл. [16]
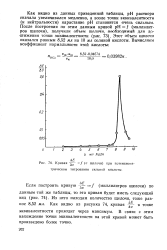 |
Кривая - д - / ( v щелочи при потенциоме-трическом титровании сильной кислоты. [17] |
В связи с этим нахождение точки эквивалентности на этой кривой может быть произведено более точно. [18]
Должен существовать удовлетворительный метод нахождения точки эквивалентности. Наиболее удобным обычно бывает применение визуального индикатора, но во многих случаях подходящего индикатора нельзя найти. [19]
Должен существовать удовлетворительный метод нахождения точки эквивалентности. [20]
Метод адсорбционного титрования применяется для нахождения точки эквивалентности при добавлении к раствору какой-нибудь соли АВ раствора другой соли CD, дающей с первой нерастворимый осадок. В титруемый раствор добавляют в небольшом количестве органический краситель, способный давать мало растворимую соль с тем ионом прибавляемой соли, который входит в состав осадка. [21]
Для достижения большей точности при нахождении точки эквивалентности следует проводить более двух определений для каждой из пересекающихся прямых. [22]
Чаще всего эти кривые строят для нахождения точки эквивалентности какой-нибудь реакции. [23]
При титровании слабых кислот и оснований нахождение точки эквивалентности, ( см. рис. 3, б) представляет известные трудности. [24]
Чаще всего эти кривые строят для нахождения точки эквивалентности какой-нибудь реакции. [25]
Кондуктометрия - это метод электрохимической индикации, в котором для нахождения точки эквивалентности используют изменение электропроводности в ходе титрования. [26]
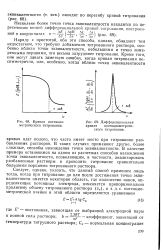 |
Кривая потенцио-метрического титрования. [27] |
В таких случаях применяют другие, более сложные, способы нахождения точки эквивалентности. [28]
Титриметрические ( в т.ч. рН - метрический) методы определения кислот основаны на нахождении точки эквивалентности. Однако в ряде, случаев целесообразно прекратить титрование задолго до эквивалентной точки. Это возможно при применении рН - статического метода. [29]
Особенно это относится к титрованию не до определенного значения рН, а при нахождении точки эквивалентности по перегибу кривой титрования, когда зачастую обращают внимание лишь на потенциал, но не на рН раствора. [30]
Страницы: 1 2 3 4