Нахождение - электрон
Cтраница 1
Нахождение электрона на более удаленной орбите обусловливается большим запасом потенциальной энергии, и поэтому, естественно, переход электрона на ту или иную дальнюю орбиту может быть совершен только при поступлении энергии извне, например, при столкновении атома с другим атомом или молекулой при электронной бомбардировке или при сообщении атому других видов энергии. Чем больше величина поглощенной атомом энергии, тем на более удаленную орбиту переходит электрон. Состояние атома, при котором электрон находится на более удаленной орбите, называют возбужденным. [1]
 |
Энергия, длина и порядок связи двухатомных гомоядерных молекул элементов 1-го периода.| Контурные диаграммы электронной плотности связывающей ( а и разрыхляющей ( б орбиталей в H2h. [2] |
Нахождение электрона на связывающей орбитали обусловливает сокращение межъядерного расстояния и упрочнение молекулы. [3]
Нахождение электронов на молекулярной несвязывающей г - орбитали соответствует концентрации избыточного отрицательного заряда на концевых атомах. [4]
Нахождение электронов водорода в электронном газе соответствующей решетки металла дает основание говорить в таких случаях о металлическом типе связи водорода. Этот тип химической связи полностью реализуется лишь в гидридах переходных металлов VI-VIII групп. Основной причиной этого перехода от металлического к ионному типу связи следует считать уменьшение электроотрицательности металлов при продвижении влево по периоду и, как следствие, оттягивание валентных электронов металлов к атому водорода. В то же время гидриды переходных металлов I и II групп, также как непереходных металлов III группы занимают промежуточное положение между солеобразньши гидридами и летучими гидридами непереходных элементов V, VI и VII групп. В этом же направлении, начиная с типично металлических гидридов, наблюдается плавный переход и в типе связи - от металлической к атомной связи: валентные электроны атома водорода во все большей степени оттягиваются к его партнеру по связи вследствие возрастания электроотрицательности последнего. Таким образом, оказывается, что у гомеополярных гидридов элементов главной подгруппы VII группы атом водорода поляризован положительно. [5]
Нахождение электронов молекулы Н2 на связующей молекулярной орбитали приводит к понижению энергии атомов и образованию связи между ними. Переход электронов на щую орбиталь ослабляет связь. Молекула в этом состоянии на и самопроизвольно распадается на атомы. [6]
Вероятность нахождения электронов, или плотность электронного облака, определяется квадратом волновой функции ( см. гл. [7]
Вероятность нахождения электрона 1 в пространственно-спиновом элементе объема dx при произвольном положении остальных электронов определяется путем интегрирования выражения (11.13) по координатам второго и всех следующих ( вплоть до п-то) электронов. Разумеется, нас больше интересует вероятность нахождения любого из п электронов в элементе dx, потому что электроны в данной системе неразличимы. [8]
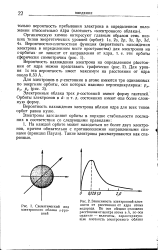
Вероятность нахождения электрона в точке на расстоянии 50 пм от яара в некотором определенном направлении составляет только 15 % вероятности нахождения его у самого ядра. Вероятность нахождения электрона в том же объеме на расстоянии 1 мм в точности не равна нулю, но она столь мала ( - 10 в степени - 2 - Ю7), что ею можно полностью пренебречь. [9]
Вероятность нахождения электрона 1 в пространственно-спиновом элементе объема dx при произвольном положении остальных электронов определяется путем интегрирования выражения (11.13) по координатам второго и всех следующих ( вплоть до п-го) электронов. Разумеется, нас больше интересует вероятность нахождения любого из п электронов в элементе dx, потому что электроны в данной системе неразличимы. [10]
Вероятность нахождения электрона вблизи ядра для всех типов орбит равна нулю. [12]
 |
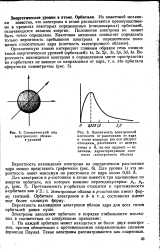
Схематический вид [ IMAGE ] Зависимость электронной. [13] |
Вероятность нахождения электрона вблизи ядра для всех типов орбит равна нулю. [14]
Страницы: 1 2 3 4 5