Негибридизованная
Cтраница 1
Негибридизованная 2р2 - АО находится в перпендикулярной плоскости. [2]
 |
Образование трех гибридных зр2 - орбиталей. [3] |
Негибридизованная р-орбиталь одного атома углерода перекрывается с р-орбиталью второго углеродного атома. Длина углерод-углеродной связи в этом случае составляет 0 134 нм. [4]
 |
Схема образования о-связей ( а и л-связей ( б в молекуле этилена. [5] |
Негибридизованная р-орбиталь атома ( на рисунке не показана) направлена перпендикулярно к плоскости гибридных орбиталей. [6]
Негибридизованная р-орбиталь атома азота перекрывается еще с двумя р-орбиталями атомов кислорода, образуя делокализованную л-связь. [7]
Оставшаяся негибридизованная р-орбиталь расположена перпендикулярно этой плоскости. Гибридные орбитали образуют cr - связи, имеющие максимум перекрывания на линии, соединяющей центры атомов, а ттегибридезованкые р-орбитали - г п-связь, имеющую два максимума перекрывания по обе стороны от плоскости молекулы. [8]
Однако негибридизованная р-орбиталь благодаря своей симметрии может пересекаться с двумя р-орбиталями соседних атомов. В результате возникают тг-орбитали, охватывающие несколько атомов, - делока-лизованные тг-орбитали. В этой молекуле каждый атом углерода образует три очжязи, в образовании которых принимают участие sp - орбитали. Кроме того, имеется делокализованная тг-система, охватывающая всю молекулу; дело-кализованную орбиталь занимают шесть электронов. Молекула является правильным шестиугольником. Первый способ отражает эквивалентность связей в молекуле. Второй способ - с помощью чередующихся одинарных и двойных связей - не отражает эквивалентности связей в молекуле бензола. Однако он используется чаще, особенно при изображении более сложных сопряженных систем. [9]
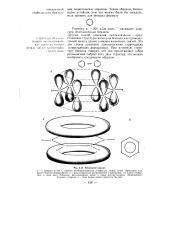 |
Бензольное кольцо. [10] |
С имеется негибридизованная р-орбиталь; между этими обриталями возникав. [11]
С - С в бензоле равны, поэтому негибридизованная р-орби-та, несомненно, перекрывается не только с негибридизованной р-орбнтой правого или левого атома углерода, но одновременно и с орбитами обоих соседних атомов. Понятно, что в такой молекуле характер связи С - С должен отличаться как от простой, так и от двойной связи, и все атомы углерода должны быть равноценными. [12]
Таким образом, у каждого из атомов углерода остается одна негибридизованная 2р - орбиталь, перпендикулярная плоскости, в которой находятся атомы углерода и водорода. [13]
 |
Молекула метана.| Молекула этана.| Молекула этена. [14] |
Оси гибридных зр2 - орбиталей атома углерода пересекаются под углом 120, а негибридизованная 2р - орбиталь перпендикулярна плоскости, в которой лежат эти оси. [15]
Страницы: 1 2
