Негибридизованная
Cтраница 2
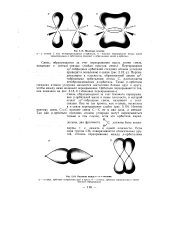 |
Молекула этилена.| Различие между о - и л-связями. [16] |
Перпендикулярно к плоскости, образованной двумя sp2 - гибридными орбиталями атома С, расположена негибридизованная р-орбиталь. [17]
В активированном комплексе атом углерода переходит в состояние sp1 - гибридизации, причем его негибридизованная р-орбиталь перекрывается как с ВЗМО нуклеофила, так и с ВЗМО уходящей группы - бромид-иона. [18]
Указанные перестройки одной 2х - орбитали и трех 2р - орби-талей выгодны, так как в случае хр2 - гибридизации становится доступной одна негибридизованная р-орбиталь ( см. разд. Реализуется-тот способ гибридизации, при котором атом углерода может образовать максимально прочные связи, а другие связываемые с ним атомы ( и электронные пары, образующие эти связи) возможно дальше отстоят друг от друга, так что общая внутренняя энергия полученного соединения оказывается минимальной. [19]
При этом каждый атом С связан с тремя другими благодаря перекрыванию гибридных орбиталей. Негибридизованная одна р-орбиталь располагается по обе стороны плоскости гибридных 5р2 - орбиталей. [20]
 |
Образование а - и я-связей 3G. [21] |
Возможны два других типа гибридизации, в которых не участвуют одна или две р-орбитали. Во-первых, возможна 5р2 - гибриди-зация, в результате которой образуется три яр2 - гибридные орбита-ли и остается одна негибридизованная р-орбиталь. [22]
Если гибридизация проводится в препаративном варианте, то при выборе метода прежде всего учитывают природу образца. Это могут быть: 1) РНК, участвующая в образовании гибрида; 2) интактпый гибрид; 3) ДНК, входящая в состав гибрида, или 4) негибридизованная РНК. [23]
Описание электронной структуры каждой структуры Кекуле на основе теории Слейтера - Полин-га сводится к использованию тех рассуждений, которые уже были приведены при рассмотрении молекулы С2Н4 ( стр. Такое описание впервые было предложено Хюккелем [584]: при гибридизации только двух 2р - орбиталей каждого атома С с 25-орбиталью получаются три тригональные орбитали, оси которых расположены в плоскости ху ( см. стр. У каждого атома углерода остается одна негибридизованная орбиталь 2р2, ось которой перпендикулярна плоскости ху. Три тригональные орбитали каждого из шести атомов углерода комбинируют попарно друг с другом и с ls - орбита-лями атомов Н, образуя двенадцать локализованных орбита лей валентных связей, каждая из которых занята двумя электронами. [24]
Страницы: 1 2