Sd-металл
Cтраница 1
Соединения Sd-металлов в их низших степенях окисления с водородом, бором, углеродом, азотом, кремнием и фосфором, как правило, обладают необычными стехиометрией и кристаллической структурой. Их химия представляет интерес в специальных областях, таких, как новая керамика, и здесь рассматриваться не будет. Из бинарных соединений наибольшее общее значение имеют оксиды, сульфиды и галогениды, а также их производные. [1]
Диаграммы легких Sd-металлов с 4d - и Srf-металлами существенно отличаются от диаграмм между Ы - и 5с / - аналогами. [2]
Устойчивые аквакатионы Sd-металлов играют ключевую роль в неорганической и бионеорганической химии этих элементов. [3]
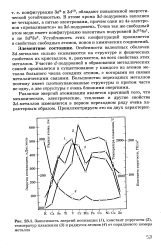 |
Зависимость энергий ионизации ( 1, констант упругости ( 2, температур плавления ( 3 и радиусов атомов ( 4 от порядкового номера металла. [4] |
Особенности валентных оболочек Sd-металлов сильно сказываются на структуре и физических свойствах их кристаллов, и, разумеется, на всех свойствах этих металлов. Участие d - подуровней в образовании металлических связей проявляется в существовании у каждого из атомов металла большого числа соседних атомов, с которыми он связан металлическими связями. Большинство переходных металлов поэтому имеет плотноупакованные структуры и притом часто не одну, а две структуры с очень близкими энергиями. [5]
Оксиды М2О3 образуют все Sd-металлы, за исключением никеля и цинка. Их также получают из солей осаждением гидроксидов М ( ОН) 3 и последующим прокаливанием. Они представляют собой темные с оттенками или черные кристаллические вещества, нерастворимые в воде и растворимые в кислотах. [6]
 |
Слой в структуре NaBr - 2H20. [7] |
Структуры дигидратов некоторых дигалогени-дов Sd-металлов построены из сочлененных ребрами октаэдри-ческих цепочек МХ4 ( рис. 15.16 5); такую структуру имеют дих-лориды и дибромиды марганца, железа, кобальта и никеля. [8]
Нитраты Mg и многих Sd-металлов обычно получаются в виде гидратов. Последние представляют собой обычные ионные кристаллы, в то время как безводные соли во многих случаях оказываются неожиданно летучими и более трудными для синтеза. Нагревание многих нитратных гидратов приводит к образованию гидроксосолей или оксидов, но летучие безводные нитраты многих переходных и менее электроположительных металлов ( Be, Mg, Zn, Hg, SnIV, Tilv) могут быть получены действием жидкого N2Os или смеси N2O4 и этилацетата на металл или какое-либо его соединение. [9]
Различие координационных сфер гидратированных катионов Sd-металлов определяет различную устойчивость и энергии гидратации. Различия в строении координационных сфер сильно сказываются на среднем времени жизни молекул Н20 в аквакатионах. [10]
Например, катионы первого переходного ряда ( Sd-металлов) образуют комплексы с этилендиамином, ПЭПА и анионитами, синтезированными на основе ПЭПА, константы устойчивости которых понижаются в указанной последовательности. [11]
Хотя табл. 23.2 демонстрирует близость свойств лишь для Sd-металлов, характеристики 4d - и Sd-метал-лов почти полностью умещаются в интервалы числовых значений, приведенные в табл. 23.2. При этом свойства элементов, расположенных в каждой из В-подгрупп, особенно близки. [12]
Влияние процессов упорядочения на температурный ход восприимчивости сплавов на основе Sd-металлов слабо изучено, однако, как видно из результатов [5, 6], оно может быть в ряде случаев причиной существенного изменения магнитного состояния, а соответственно С и вр. [13]
В ряде случаев обнаружен параллелизм между каталитической активностью ( по разложению Н2Ог) и кроветворной активностью координационных соединений Sd-металлов. [14]
Во втором параграфе центральной части обзора ( § 6) описаны свойства интерметаллидов РЗМ - переходный d - металл, и в первую очередь Sd-металл, в особенности марганец, железо, кобальт и никель. В силу того что ионы многих d - металлов, как правило, магнитно-активны, естественно ожидать гораздо более сложного их влияния на кристаллографические структуры этих соединений. Следует также еще раз подчеркнуть, что наиболее детальное изучение соединений РЗЭ с 3 -металлами от марганца до никеля ( с Sd-металлами, стоящими слева от марганца - от скандия до хрома - интерметаллиды с РЗМ не образуются) стимулировалось поиском новых, более совершенных высококоэрцитивных материалов для постоянных магнитов. Вначале автор рассматривает изученные фазовые диаграммы с различными типами интерметаллических соединений. Затем переходит к обзору результатов исследований их магнит-дых свойств. [15]
Страницы: 1 2