Нейтрализация - сильная кислота
Cтраница 2
При нейтрализации сильной кислоты концентрация ее анионов остается постоянной в течение всего процесса титрования. Если нейтрализуют кислоты с рКа sS 3, равновесные концентрации анионов кислот с начала титрования достаточно велики. В процессе титрования этих кислот концентрация их анионов до точки эквивалентности нелинейно увеличивается, что особенно заметно для сравнительно сильных кислот. При нейтрализации слабых кислот с р / Са 5 в случаях, когда реакция нейтрализации протекает количественно, концентрация анионов до точки эквивалентности линейно увеличивается, а затем после точки эквивалентности остается постоянной, равной концентрации титруемой кислоты. Гидролиз соли вызывает уменьшение концентрации анионов вблизи точки эк-вивадентности. Очень слабые кислоты даже при избытке сильного основания содержат большое количество недиссоциированных молекул НАп, а концентрация их анионов остается ниже концентрации титруемой кислоты. [16]
При нейтрализации сильных кислот и оснований теплота нейтрализации почти одинакова. [17]
При нейтрализации сильных кислот едкий натр часто заменяют содой. [18]
Для нейтрализации сильных кислот, кальциевые соли которых хорошо растворимы в воде, может быть использован любой из указанных выше реагентов. [19]
При нейтрализации сильных кислот, кальциевые соли которых труднорастворимы в воде, эти соли не только выпадают в осадок, но при больших концентрациях могут отлагаться на поверхности нейтрализующего материала, что тормозит ход реакции. [20]
При нейтрализации сильных кислот, кальциевые соли которых трудно растворимы в воде, эти соли не только выпадают в осадок, но при больших концентрациях могут отлагаться на поверхности нейтрализующего материала, что тормозит ход реакции. [21]
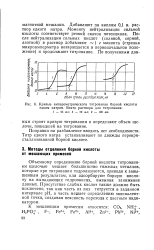 |
Кривые амперометрического титрования борной кислоты едким натром. Взято раствора для титрования. [22] |
Моменту нейтрализации сильной кислоты соответствует резкий скачок потенциала. После нейтрализации сильных кислот ( соляной, серной, азотной) в раствор добавляют - 1 г маннита ( стрелка микроамперметра возвращается в первоначальное положение) и продолжают титрование. [23]
Теплоты нейтрализации сильных кислот и оснований в отсутствие воды также отличаются от значения, равного - 13 7 ккал / моль. [24]
Теплота нейтрализации сильной кислоты сильным основанием в разбавленных растворах равна 13 7 ккал. [25]
 |
Растворимость важнейших солей в воде. [26] |
Однако при нейтрализации сильной кислоты слабым основанием, слабой кислоты сильным или слабым основанием тепловые эффекты положительны, но различны по величине. [27]
Однако при нейтрализации сильной кислоты слабым основанием, слабой кислоты сильным или слабым основанием тепловые эффекты различны. [28]
Обычная реакция нейтрализации сильной кислоты сильным основанием протекает одинаково как в водном растворе, так и в жидком аммиаке. [29]
Постоянство теплоты нейтрализации сильных кислот v оснований, равной теплоте образования воды из ионов Н и ОН - ( 13650 кал), прямо указывает на ионный характер реакции нейтрализации. [30]
Страницы: 1 2 3 4