Нейтрализация - слабое основание
Cтраница 1
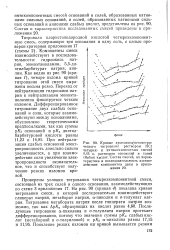
Нейтрализация слабых оснований - диэтиламина, моноэтаноламина и гидразина, наоборот, вызывает повышение электропроводности раствора. В случае титрования смесей, содержащих диэтиламин и моноэтаноламин в начале титрования на кривой наблюдается небольшой минимум. На участке кривой между первым и вторым изломами электропроводность раствора немного увеличивается, что характерно для взаимодействия ацетата с хлористоводородной кислотой. Избыток титранта вызывает сильное увеличение электропроводности раствора. [1]
При нейтрализации слабых оснований электропроводность довольно сильно увеличивается, а при взаимодействии соли увеличение электропроводности незначительное, что и способствует получению резких изломов кривой. [3]
При нейтрализации слабого основания сильной кислотой или наоборот протекают одновременно два процесса: а) диссоциация слабого электролита с соответствующим тепловым эффектом АЯдиСС и б) процесс нейтрализации. [4]
 |
Кривая нейтрализации 0 1 н. раствора аммиака 0 1 н. раствором НО. [5] |
Кривая нейтрализации слабого основания сильной кислотой несимметрична в отношении точки нейтрализации. [6]
 |
Титрование 0 1 н. раствора аммиака 0 1 н. раствором НС1. [7] |
Кривая нейтрализации слабого основания сильной кислотой несимметрична в отношении точки нейтральности. [8]
Реакция нейтрализации слабого основания является заметно обратимой, и в растворе в момент эквивалентности имеются непрореагировавшие ионы водорода. В принципе, положение здесь аналогично нейтрализации слабой кислоты сильными основаниями. [9]
 |
Кривая нейтрализации 0 1 и. раствора аммиака 0 1 н. раствором НС1. [10] |
Кривая нейтрализации слабого основания сильной кислотой несимметрична в отношении точки нейтрализации. [11]
Аналогично при нейтрализации слабого основания эквивалентным количеством сильной кислоты не все основание будет нейтрализовано. [12]
 |
Теоретические кривые кон-дуктометрического титрования сла. [13] |
В случае нейтрализации слабого основания слабой кислотой зависимости, характеризующие кислотно-основные равновесия, представляются в следующем виде. [14]
Почему значения теплот реакций нейтрализации разных слабых оснований и слабых кислот различаются. [15]
Страницы: 1 2 3