Нейтрализация - водный раствор
Cтраница 2
Соли фторборной кислоты могут получаться также нейтрализацией водных растворов этой кислоты соответствующими основаниями или растворением окислов металлов в кислоте. При нагревании они снова сравнительно легко отщепляют фтористый бор [7-10] и поэтому часто служат исходным сырьем для его получения, как описано в первой главе. [16]
Азиды рубидия и цезия могут быть получены при нейтрализации водных растворов МеОН или Ме2СО3 азотистоводородной кислотой. [17]
Ввиду димерпзации молекул ( H2F2) кислота является слабой. При нейтрализации водного раствора кислоты сначала образуется кислая соль, например гидродифторид калия KHF2, затем нормальный фторид KF. Для HF характерно образование кристаллических соединений, которые хорошо плавятся и кристаллизуются без разложения, например K. [18]
Кислые растворы тиооксината калия сохраняются довольно продолжительное время. При нейтрализации водного раствора калиевой соли соляной кислотою выпадают красные криста. Солянокислая соль в твердом состоянии представляет собою лимонно-желтые кристаллы, легко разлагающиеся водою с образованием красного дигидрата тиооксина. [19]
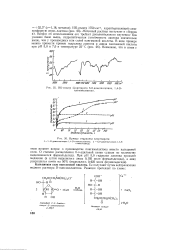 |
ИК-спектр хлоргидрата 6 - 0-диметилглицил, 1 4 - D-глюконолактона.| Кривые гидролиза хлоргидрата. [20] |
Ее получают путем нейтрализации водного раствора D-пангамолактона. [21]
Понятия гомогенности и гетерогенности нужно отличать от понятий гомофазности и гетерофазности. Так, например, реакция нейтрализации водного раствора щелочи раствором кислоты является гомогенным гомофазным процессом. Реакция взаимодействия газообразных НС1 и NH3 с образованием кристалликов ( дыма) МН4С1 относится к гомогенно-гетерофазным процессам. [22]
Некоторые соли технециевой кислоты - пертехнетаты - получены в вееомых количествах. Например, пертехнетат аммония получен нейтрализацией водного раствора Тс2О7 аммиаком, а также при растворении TcaSy в смеси аммиака и перекиси водорода. [23]
Простейший из них заключается в обменной реакции или нейтрализации водного раствора кислоты подходящим основанием. [24]
Аналогичным методом синтезируют из антрахинон-1 5-дисульфоната 1 5-диаминоантрахинон. Смесь 103 кг антрахинон-1 5-дисульфоната натрия и 700 л водной диаммонийной соли мышьяковой кислоты ( полученной нейтрализацией водного раствора 14 2 кг мышьяковой кислоты аммиаком до рН7 и разбавлением водой до объема в 700 л) размешивают и нагревают в автоклаве. В течение 30 мин поддерживают температуру 190 С, затем 30 мин-200 С, 30 мин-210 С и, наконец, в течение 24 ч - 220 С. Содержимое автоклава охлаждают до комнатной температуры и реакционную массу фильтруют. [25]
Аналогичным методом синтезируют из антрахинон-1 5-дисульфоната 1 5-диаминоантрахинон. Смесь 103 кг антрахинон-1 5-дисульфоната натрия и 700 л водной диаммонийной соли мышьяковой кислоты ( полученной нейтрализацией водного раствора 14 2 кг мышьяковой кислоты аммиаком до рН7 и разбавлением водой до объема в 700 л) размешивают и нагревают в автоклаве. В течение 30 мин поддерживают температуру 190 С, затем 30 мин-200 С. [26]
Сущность метода определения двуокиси хлора и хлора в водном растворе основана на тех же реакциях, что и газовый анализ. Однако определение водного раствора двуокиси хлора требует предварительной нейтрализации раствора с помощью буферного раствора. Стадия нейтрализации водного раствора необходима, поскольку для обеспечения нормальных условий абсорбции газовоздушной смеси двуокись хлора - хлор используется вода, подкисленная соляной кислотой. [27]
Сущность метода определения двуокиси хлора и хлора в водной растворе основана на тех же реакциях, что и газовый анализ. Однако определение водного раствора двуокиси хлора требует предварительной нейтрализации раствора с помощью буферного раствора. Стадия нейтрализации водного раствора необходима, поскольку для обеспечения нормальных условий абсорбции газовоздушной снеси двуокись хлора - хлор используется вода, подкисленная соляной кислотой. [28]
Сущность метода определения двуокиси хлора и хлора в водной растворе основана на тех же реакциях, что и газовый анализ. Однако определение водного раствора двуокиси хлора требует предварительной нейтрализации раствора с помощью буферного раствора. Стадия нейтрализации водного раствора необходима, поскольку для обеспечения нормальных условий абсорбции газовоздушной смеси двуокись хлора - хлор используется вода, подкисленная соляной кислотой. [29]
Реакцию солеобразования часто используют для выделения и очистки аминов. Например, анилин не растворим в воде, но растворяется в хлороводородной кислоте, так как превращается в аммониевую соль. Это позволяет отделить анилин от примеси не растворимых в воде органических соединений. Нейтрализация водного раствора приводит к выделению анилина в виде свободного основания. [30]
Страницы: 1 2 3