Полная нейтрализация - кислота
Cтраница 2
После этого через воронку / налить в колбу 3 достаточное для полной нейтрализации кислоты количество раствора едкого натра и заменить воронку 1 стеклянной палочкой. [16]
Другим примером, часто встречающимся на практике, является невозможность достичь полной нейтрализации кислот или оснований ( вследствие сольволиза их солей), несмотря на, казалось бы, эквивалентное количество добавленного нейтрализующего реагента в процессе их взаимодействия. [17]
Это значит, что из 20 мл щелочи, потребных для полной нейтрализации кислоты, для увеличения рН на единицу надо прилить 18 мл. [18]
Реакция нейтрализации кислоты до Na3PO4 сильно обратима, и излом кондуктометрической кривой, фиксирующий полную нейтрализацию кислоты, не обнаруживается. Поэтому кондуктометрическое определение фосфорной кислоты основывается на нейтрализации первого кислотного эквивалента. [19]
Поэтому не следует использовать смеси с высоким содержанием НС1 и HF и при осуществлении процесса допускать полную нейтрализацию кислоты. [20]
При титровании двухосновных кислот средней силы кондуктометрические кривые имеют один пологий минимум: излом кривой обычно соответствует полной нейтрализации кислоты, даже если константы диссоциации по первой и второй ступеням заметно различаются. [21]
При отношении HF: SiF4, меньшем 1: 12, уже возможно использование мела 176, позволяющего достичь полной нейтрализации кислоты. [22]
Поэтому количество кислоты в анализируемом образце можно определить, измерив количество раствора основания с известной концентрацией, которое требуется для полной нейтрализации кислоты. Такой способ называется титрованием и широко используется как стандартный аналитический прием. Нормальностью N раствора кислоты или основания называется число их эквивалентов в 1 л раствора. [23]
Ингибированная кислота может отрицательно влиять на при-забойную зону, особенно порового пласта: Следует учитывать, что ингибитор ПБ-5 после полной нейтрализации кислоты может оставаться в поровом пространстве пласта в виде хлопьевидной объемистой органической массы. При использовании 15 - 20 % ингибированной кислоты может выпасть 5 - 7 кг осадка на 1 м3 закачанного в пласт раствора. При неполной нейтрализации кислоты такого осадка не выделяется. Следовательно, при обработке поровых коллекторов нецелесообразно выдерживать кислоту в пласте до полной ее нейтрализации. [24]
Чтобы, например, определить концентрацию кислоты, выделяют известный объем исследуемого раствора и постепенно прибавляют раствор щелочи известной концентрации до полной нейтрализации кислоты. Зная объем добавленной щелочи, легко рассчитать концентрацию раствора кислоты. Следовательно, экспериментальная задача состоит в определении точки эквивалентности, которая соответствует точной нейтрализации кислоты щелочью. [25]
 |
Изменение рН растворов А12 ( 084 з с изменением кислотности. [26] |
Таким образом, титрование свободной кислоты в присутствии гидролизующихся солей затруднительно, поскольку гидроокиси этих металлов начинают выделяться из раствора ранее достижения полной нейтрализации кислоты. [27]
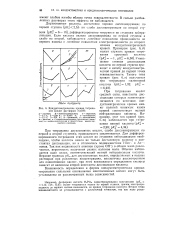 |
Кондуктометрические кривые титрования кислот раствором NaOH. [28] |
При титровании кислот средней силы, константы диссоциации которых заметно различаются по величине, кон-дуктометрические кривые имеют пологий минимум: излом кривой соответствует полной нейтрализации кислоты. [29]
Уксусную кислоту добавляли в количестве 2 - 3 %, она необходима для предотвращения выпадения треххлористого железа в виде объемного осадка гидроокиси железа при полной нейтрализации кислоты карбонатами. Добавка уксусной кислоты весьма существенно снижает скорость реакции. [30]
Страницы: 1 2 3 4