Неметалличность
Cтраница 2
Активнее всего протекает химическое взаимодействие атомов с высокой металличностью и атомов, обладающих высокой неметалличностью, вследствие их крайне противоположных тенденций к процессам приема - отдачи электронов. Процесс взаимодействия этих веществ обычно протекает экзотермически и создания особых условий не требует. Полученные в результате такого активного взаимодействия химические соединения являются очень прочными и проявляют большую устойчивость к окислительно-восстановительным процессам. [16]
Как изменяются радиус атомов, энергия ионизации, сродство К электрону, электроотрицательность, металличность и неметалличность элементов в малых периодах. [17]
Вообще говоря, сила высшей кислородной кислоты, отвечающей данному неметаллу, не может служить мерилом степени его неметалличности; так, селеновая кислота вследствие несколько большего размера ее аниона в сравнении с ионом SCU - должна быть несколько сильнее серной, хотя селен - менее резко выраженный неметалл в сравнении с серой. Этот вывод послужил поводом для экспериментального определения второй константы диссоциации HzSeO4, которая действительно оказалась в 1 6 раза больше, чем вторая константа диссоциации серной кислоты. [18]
Окислительная активность падает при переходе от кислорода к тяжелым элементам - Se, Те, Ро - в полном соответствии с уменьшением неметалличности, и если кислород способен, например, взаимодействовать с подавляющим большинством элементов при тех или иных условиях, то селен и теллур - лишь с весьма немногими наиболее активными металлами и неметаллами. [19]
Вследствие незначительной разницы в тенденции к процессу приема - отдачи электронов еще менее активно взаимодействуют: а) металлы с низкой металлично-стью и неметаллы с низкой неметалличностью, б) неметаллы с низкой неметалличностью. [20]
При анализе химических свойств элементов ясно прослеживается основная диалектическая закономерность - единство противоположностей: в каждом химическом элементе имеется сочетание двух противоположных начал - металличности и неметалличности, восстановительных и окислительных свойств. [21]
Сравнение температур плавления и температур кипения веществ в ряду F2 - CJ2 - Вг2 - 12 - At2 указывает на закономерное изменение свойств в сторону снижения неметалличности и появления металлических признаков. [22]
Вследствие незначительной разницы в тенденции к процессу приема - отдачи электронов еще менее активно взаимодействуют: а) металлы с низкой металлично-стью и неметаллы с низкой неметалличностью, б) неметаллы с низкой неметалличностью. [23]
Исходя из так называемого представления о пассивном сопротивлении, предложенном еще Вернером, И. И. Черняев формально приписал каждому элементу величину е, коэффициент пассивного сопротивления, который, по его мнению, весьма чувствителен к степени неметалличности данного элемента. [24]
Что является количественной характеристикой неметалличности. [25]
Сопоставляя значения относительных электроотрицательностей элементов от франция ( 0 86) до фтора ( 4 10) ( см. табл. 2.2), легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением номера элемента, в группе - уменьшается. Ее значения служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. [26]
Сопоставляя их, легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением порядкового номера элемента, в подгруппе - уменьшается. Эти значения служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицатель-ность, тем сильнее элемент проявляет неметаллические свойства. [27]
Сопоставляя значения электроотрицательностей элементов от франция ( 0 86) до фтора ( 4 10) ( табл. 2.2), легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением номера элемента, в группе - уменьшается. Ее значения служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. [28]
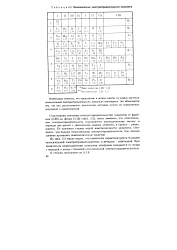 |
Относительные элеотроотрицателыюсти элементов. [29] |
Сопоставляя значения электроотрицателыюстей элементов от франция ( 0 86) до фтора ( 4 10) ( табл. 2.2), легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением номера элемента, в группе - уменьшается. Ее значения служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. [30]
Страницы: 1 2 3 4