Неметалличность
Cтраница 3
Сопоставляя их, легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением порядкового номера элемента, в подгруппе - уменьшается. Эти значения служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. [31]
Выводы, сделанные с различных точек зрения, не всегда совпадают; так, олово и свинец - металлы по структуре простых веществ, отвечающих этим элементам, и неметаллы по способности их атомов принимать электроны. Переход от одного полюса свойств ( металличность) к другому ( неметалличность) совершается от элемента к элементу цостепенно и отнести однозначно некоторые элементы к той или другой категории не всегда возможно. [32]
Выводы, сделанные с различных точек зрения, не всегда совпадают; так, олово и свинец - металлы по структуре простых веществ, отвечающих этим элементам, и неметаллы по ряду других свойств их атомов. Переход от одного полюса свойств ( металлич-ность) к другому ( неметалличность) совершается от элемента к элементу постепенно, и отнести однозначно некоторые элементы к той или другой категории не всегда возможно. Попытки четкого разграничения элементов на металлы и неметаллы следует в принципе считать метафизическими. Почти всем элементам в большей или меньшей степени присуща амфотерность ( дву-природность) - в широком понимании этого слова. [33]
В соответствии с изменениями потенциалов ионизации в периодах и группах в общем происходит относительное изменение свойств элементов. Однако потенциал ионизации не может служить единственной количественной мерой относительной металличности или неметалличности элементов. Действительно, самым высоким потенциалом ионизации обладает атом гелия, но так как он относится к инертным элементам, говорить о характере его свойств довольно трудно. Далее, если рассмотреть изменение потенциала ионизации в пределах второго периода ( см. рис. 8, Li - He), то обнаруживаются скачки. Потенциал ионизации у кислорода оказывается меньше, чем у азота. Такие скачки, связанные с некоторыми особенностями строения внешних электронных оболочек атомов, наблюдаются и в остальных периодах, хотя неметаллические свойства нарастают. [34]
Радиусы атомов этих элементов уменьшаются слева направо. Уменьшение радиуса атомов и увеличение числа электронов на внешнем слое являются причиной уменьшения металличности и увеличения неметалличности элементов слева направо. [35]
Анализируя получившееся расположение элементов, Менделеев заметил, что по вертикалям его системы, в которых расположены элементы самого различного характера ( металлы, неметаллы, элементы с промежуточными свойствами), атомные веса возрастают сверху вниз, как правило, малыми более или менее равномерными скачками. Очевидно, именно такова закономерность изменения атомных весов элементов при постепенном переходе от одного полюса свойств их ( металличность) до другого ( неметалличность), делает вывод Менделеев. По горизонталям же системы Менделеева атомные веса слева направо увеличиваются резкими, все возрастающими скачками. Очевидно, именно такова закономерность изменения атомных весов в любом ряду сходных элементов, снова заключает Менделеев. Эти закономерности выражают, разумеется, неизвестный еще общий закон, по которому развивается материя. И Менделеев, поняв, что это действительно закономерности, сейчас же использует их для неожиданно смелых выводов. [36]
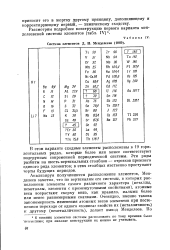 |
Система элементов Д. И. Менделеева ( 1869. [37] |
Анализируя получившееся расположение элементов, Менделеев заметил, что по вертикалям его системы, в которых расположены элементы самого различного характера ( металлы, неметаллы, элементы с промежуточными свойствами), атомные веса возрастают сверху вниз, как правило, малыми более или менее равномерными скачками. Очевидно, именно такова закономерность изменения атомных весов элементов при постепенном переходе от одного полюса свойств их ( металличность) к другому ( неметалличность), делает вывод Менделеев. [38]
Периодом называется совокупность элементов, расположенных в порядке постепенного возрастания атомных весов, начинающаяся с типично металлического элемента ( щелочного металла) и заканчивающаяся типично неметаллическим элементом ( галогеном); заключительный элемент каждого периода - инертный газ. Таким образом, на протяжении каждого периода проходит вся гамма оттенков в характере элемента от одного полюса свойств ( типичная металличность) до противоположного полюса свойств ( типичная неметалличность) и до третьего полюса ( химическая инертность), причем по пути от первого полюса ко второму мы встретим элементы промежуточного между металлом и неметаллом характера, совмещающие в той или иной степени их свойства. [39]
Как видно, табл. 7 охватывает величины относительной электроотрицательности от 0 86 для франция до 4 10 для фтора. Сопоставляя их, легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением номера элемента, в группе - уменьшается. Эти величины служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. [40]
Как видно, табл. 8 охватывает величины относительной электроотрицательности от 0 86 для франция до 4 10 для фтора. Сопоставляя их, легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением номера элемента, в группе - уменьшается. Эти величины служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. [41]
Поскольку каждый галоген в периодической системе предшествует инертному или благородному газу, он является самым электроотрицательным элементом соответствующего периода. Действительно, до достижения электронной конфигурации атомов инертных и благородных газов ns2npe атомам галогенов не хватает лишь одного электрона, вследствие чего для них наиболее характерна тенденция к присоединению электрона. Тем не менее с ростом электроноемкости атомов галогенов имеет место ослабление неметалличности и, соответственно, нарастание признаков металличности. Об этом свидетельствуют уменьшение потенциалов ионизации, стандартных редокс-потенциалов и ОЭО. Если бром еще является довольно сильным окислителем, иод уже относится к числу мягких окислителей. К тому же иод представляет собой твердое вещество с металлическим блеском и проявляет заметные признаки амфотерности. [42]
Количественно сродство атома к электрону выражается энергией, затрачиваемой на отрыв электрона от однозарядного отрицательного иона. Максимальным сродством к электрону обладают атомы галогенов. Способность атомов к отдаче электронов характеризует степень металличности данного элемента, а способность к присоединению электронов - степень неметалличности элемента. Мерой относительной способности атомов в молекуле притягивать к себе электроны, т.е. приобретать отрицательный заряд, является электроотрицательность. [43]
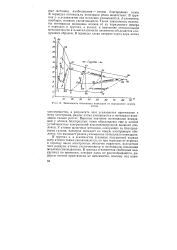 |
Зависимость потенциала ионизации от порядкового номера. [44] |
В периодах потенциалы ионизации резко возрастают. В группах s - и р-элементов они медленно уменьшаются, d - элементов, наоборот, немного увеличиваются. Такая зависимость величины потенциала ионизации атомов от их порядкового номера в периодах и группах, а значит, и изменение относительной металличности и неметалличности элементов объясняется следующим образом. [45]
Страницы: 1 2 3 4