Ненаправленность - ионная связь
Cтраница 1
Ненаправленность ионной связи ( отличие от ковалентной связи) - одно из важнейших ее свойств. Это означает, что каждый ион может притягивать к себе ионы противоположного знака по любому направлению. [1]
 |
Значения энергий смешения для некоторых стеклообразных систем. [2] |
Вследствие ненаправленности ионных связей щелочной катион стекла связан со всеми кислородными ионами данного полиэдра и прочность его закрепления в занимаемой им полости определяется способностью взаимодействовать с окружающими ионами кислорода. Сила связи щелочного иона с каждым отдельным ионом кислорода зависит от степени поляризации электронных оболочек кислородных ионов. Электронные оболочки мостикового кислорода очень сильно поляризованы двумя ионами кремния, и связь щелочного иона с ними незначительна. Немостиковый кислородный ион может дополнительно поляризоваться щелочным катионом. Таким образом, от количества немости-ковых кислородных ионов, определяемого количеством подвижных носителей, зависит скорость перемещения катионов. [3]
 |
Решетки структурных типов NaCl, CsCl и ZnO. [4] |
Ненасыщаемость и ненаправленность ионной связи приводят в большинстве ионных кристаллов к образованию структур так называемых плотнейших упаковок. [5]
Вследствие ненасыщаемости и ненаправленности ионной связи ионные координационные кристаллы характеризуются высокими координационными числами ( стр. По этой же причине высокие координационные числа ( 8, 12) имеют металлические координационные кристаллы ( стр. [7]
 |
Полярная молекула с постоянным электрическим моментом диполя. [8] |
Таким образом, вследствие ненасыщенности и ненаправленности ионной связи соединения, состоящие из ионов, представляют собой твердые тела с ионной кристаллической решеткой. [9]
Например, в кристалле Na Cl - каждый ион Na взаимодействует с 6 ионами С1 -, и наоборот / Из-за ненасыщаемости и ненаправленности ионной связи в соединениях с этой связью, как правило, образуются не молекулы, а твердые тела с ионным кристаллическим строением. [10]
 |
Решетки структурных типов NaCI, CsCl и ZnO. [11] |
Ненасыщаемость и ненаправленность ионной связи приводят в большинстве ионных кристаллов к образованию структур так называемых плотнейших упаковок. [12]
Например, в кристалле Na Cl каждый ион Na взаимодействует с 6 ионами СГ, и наоборот. Из-за ненасыщаемости и ненаправленности ионной связи в соединениях с этой связью, как правило, образуются не молекулы, а твердые тела с ионным кристаллическим строением. [13]
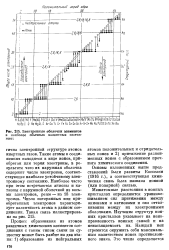 |
Электронные оболочки элементов. [14] |
Межатомные расстояния в ионных, кристаллах определяются уравновешиванием сил притяжения между анионами и катионами и сил отталкивания между их электронными оболочками. Изучение структур ионных кристаллов указывает на ненаправленность ионных связей и на ненасыщаемость их. Каждый ион стремится окружить себя максимальным количеством ионов противолож-ного знака. [15]
Страницы: 1 2 3
