Необходимость - активация
Cтраница 1
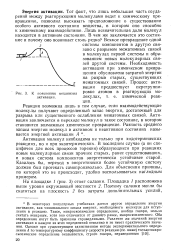 |
К пояснению механизма Ровке атомов в реагирующих мо-активации. лекулах, т. е. химической реак. [1] |
Необходимость активации при химическом превращении обусловлена затратой энергии на разрыв старых, существующих межатомных связей. [2]
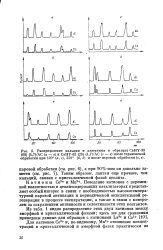
Однако вследствие, необходимости активации осуществление этой реакции также сопряжено с затратой энергии, что в равной мере относится как к термической реакции, так и к реакции, проводимой в электрическом разряде. Было показано, что в зависимости от типа разряда и условий проведения реакции устанавливается определенный предел реакции. Эти данные свидетельствуют о наличии обратной реакции разложения NH3, идущей параллельно с прямой реакцией синтеза. Выход аммиака обычно составляет несколько грамм на киловатт-час, изменяясь с изменением условий и типа разряда в пределах от десятых долей грамма до величины порядка 10 г. Наибольший выход был получен в случае тихого разряда ( 8 2 г / квт-ч), что нужно приписать более высокому давлению. Был измерен также выход аммиака, получающегося при бомбардировке смеси азота и водорода электронами заданных энергий. [3]
К недостаткам относятся также необходимость активации цементного раствора, вследствие чего в скважине долгое время нельзя проводить радиоактивный каротаж. [4]
 |
Зависимость скорости гидрирования пропиоловокислого натрия ( 0 3 г на скелетном никеле ( 0 33 г от концентрации спирта. [5] |
Наиболее общей кинетической закономерностью при гидрировании в жидкой фазе является необходимость активации обоих реагирующих компонентов на поверхности. [6]
Поведение катионов с переменной валентностью в цеолитсодержащих катализаторах представляет особый интерес в связи с необходимостью высокотемпературной паровой активации и периодической окислительной регенерации в процессе эксплуатации, а также в связи с контролем за сохранением активности и селективности этих контактов. [8]
Проведение реакций при низких и сверхнизких температурах представлялось нецелесообразным прежде всего из-за чрезвычайно малых - скоростей, обусловленных резким уменьшением множителя e - E / RT, учитывающим необходимость активации частицы перед вступлением ее в химическую реакцию. Другой трудностью, сопутствующей реакциям при низких температурах, считались специфические свойства твердого вещества, практически исключавшие возможность взаимной диффузии реагирующих частиц на сколько-нибудь значительные расстояния. [9]
К этой группе относятся, например, реакции азота с водородом и кислородом, разложение воды. G обусловлена необходимостью активации молекулы азота в каждом акте реакции. Как будет показано в главе IV, эти реакции требуют ионизации азота и, по-видимому, хотя бы частичной диссоциации. Поэтому выход NO2 не может быть больше 2 молекул а 1 ион N2, что соответствует приблизительно 6 молекулам на 100 эв. [10]
Комплексный механизм гидрирования олефинов в гетерогенном катализе представляется более вероятным. Однако, учитывая необходимость активации водорода, реакция должна осуществляться на дублете атомов катализатора. [11]
ЦСК с катионами Се3 после термопаровой обработки, и особенно после окислительной регенерации, резко теряют каталитическую активность, а кристаллическая структура при этом заметно разрушается. Интересно поведение катионов с переменной валентностью в ЦСК в связи с необходимостью высокотемпературной паровой активации и периодической окислительной регенерации катализатора, а также в связи с контролем за сохранением активности и селективности этих контактов. В [90] показано, что при окислительной регенерации происходит окисление Се3 с образованием полиядерных кислородных кластеров Се4 - О - Се4 [91], включающих мостичный некаркасный кислород, обладающий высокой подвижностью и реакционной способностью. Установлено [90], что такое окисление начинается уже при высушивании образцов на воздухе и, по-видимому, характерно для цеолитов с катионами переменной валентности. Найдено, что окисление катионов Се3 в ЦСК является обратимым процессом, однако многократное использование жестких условий обработки водородом приводит, вероятно, к дегидроксилированию поверхности и необратимому снижению активности ЦСК. Авторы показали, что высокая стабильня активность ЦСК наблюдается, если они содержат катионы церия и лантана одновременно, причем наилучшим соотношением двух этих катионов в образце является примерно равное их количество. В этом случае высокая активность сочетается с достаточной стабильностью образца. [12]
К этой группе относятся, например, реакции азота с водородом и кислородом, разложение воды. В первом случае медленность реакции и связанная с ней малая величина G обусловлена необходимостью активации молекулы азота в каждом акте реакции. Как будет показано в главе IV, эти реакции требуют ионизации азота и, по-видимому, хотя бы частичной диссоциации. Поэтому выход NO2 не может быть больше 2 молекул а 1 ион N2, что соответствует приблизительно 6 молекулам да 100 эв. [13]
Такой ряд активности обратен обычному ряду активности рассматриваемых элементов по отношению к большому числу реакций гидрирования, для которых, как правило, активность Ni Со Fe. Это связано с тем, что для осуществления синтеза аммиака на первый план выступает необходимость активации молекулы азота. [14]
Для образования таких слоев предложено довольно много составов, которые наносят обычно на плоские поверхности или изделия несложной формы окунанием или распылением. В эти составы вводят различные наполнители, облегчающие создание шероховатости, иногда - восстановители или катализаторы, исключающие необходимость активации перед химической металлизацией, или электропроводящие материалы, что позволяет сразу же наносить гальванические покрытия. Этим методом можно удобно металлизировать и такие пористые материалы, как пенопласты, бумагу, кожу. Кроме того, использование адгезионных слоев позволяет легко осуществлять селективную металлизацию. [15]
Страницы: 1 2