Необходимость - активация
Cтраница 2
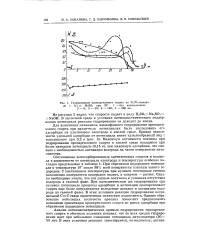 |
Гидрирование пропаргилового спирта на Pt / Pt-электро. [16] |
Для выяснения механизма жидкофазного гидрирования пропаргилового спирта при различных потенциалах была исследована его адсорбция на платиновом электроде в кислой среде. Максимум активности платины при гидрировании пропаргилового спирта в кислой среде находится при более катодном потенциале ( 0 15 в), чем максимум адсорбции, что связано с необходимостью активации водорода на части поверхности катализатора. [17]
Термохимический детектор обладает хорошей чувствительностью и малой инерционностью, простотой устройства, применением воздуха в качестве газа-носителя. Однако он имеет и ряд существенных недостатков: 1) ограниченность интервала анализируемых концентраций горючих газов; 2) ограниченность срока службы чувствительных элементов ( платиновой нити); 3) необходимость частой активации и калибровки; 4) перегорание платиновой нити при высоких ( более 4 %) концентрациях горючих газов в анализируемой смеси. [18]
При включении на разряд элементы подобно другим магниевым системам только постепенно повышают свое рабочее напряжение. У элементов, залитых пресной водой, достижение минимально допустимого напряжения отмечается только через 1 - 2 мин. В случае необходимости более быстрой активации элементы погружаются или в морскую, или в подсоленную воду. [19]
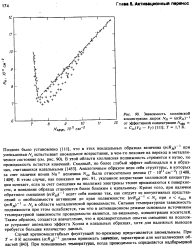 |
Зависимость холловской концентрации дырок NH ( ecRff - t от эффективной концентрации Л фф C0 ( VC - VT. Г 1 7 К. [20] |
В этой области холловская подвижность стремится к нулю, но проводимость остается конечной. В этом случае, как показано на рис. 91, указанное возрастание холловской концентрации исчезает, если за счет смещения на подложке электроны теснее прижимаются к поверхности, и поведение образца становится более близким к идеальному. Кроме того, при наличии обратного смещения ( ecRH) - l ведет себя именно так, как следует из интуитивных представлений о необходимости активации до края подвижности: ( ecRH) - l Ns при а amln и ( ecRH) - l Ns в области металлической проводимости. Сильная температурная зависимость подвижности при этом ослабляется, так что в активационном режиме основным источником температурной зависимости проводимости является, по-видимому, концентрация носителей. Таким образом, создается впечатление, что в предварительных опытах смещение на подложке устраняет аномалию эффекта Холла в идеальных образцах, хотя для надежных выводов требуется большее количество данных. [21]
Возможность адсорбции частиц такого состава на металлах группы платины предполагается и при низких анодных потенциалах в водных растворах спиртов. Однако реакция алкоксилирования на неокисленных поверхностях с заметными скоростями не протекает. Это, по-видимому, связано как с существенными различиями в структуре и энергиях адсорбции частиц одинакового состава в рассматриваемых областях потенциалов, так и с необходимостью электрохимической активации молекулы ненасыщенного органического соединения, достижимой только при высоких анодных потенциалах. [22]
Сопоставление кривых, характеризующих удельные константы скорости гидрогенолиза тиофена и величины параметра решетки сульфида металла ( dM s) ( рис. 97), показывает, что между ними существует некоторое сходство. Указанная симбатность имеет место, если реакция гидрогенолиза протекает по дублетной схеме через стадию образования реберной структуры, возможно, с участием атомов С и S. Это может быть следствием различных причин: 1) осложнение гидрогенолиза крекингом тиофена без участия водорода; 2) неодинаковая лимитирующая стадия при гидрогенолизе в присутствии различных катализаторов; 3) неизвестность точного состава активного компонента и неправомерность в связи с этим использования данных dM - s для объемных соединений; 4) неучет необходимости активации на поверхности не только тиофена, но и водорода. [23]
При реакции СО с метанолом получают уксусную кислоту. Реакцию СН3ОН СО - - СН3ООН проводят в газовой фазе при 10 - 70 МПа в присутствии катализаторов. Константа равновесия К п этой реакции уменьшается с температурой и составляет при 300, 500 и 600К: Ю13, 104 - 8 и 1026 соответственно. Поэтому проведение этой реакции при повышенных давлениях СО объясняется не термодинамическими, а кинетическими соображениями - необходимостью активации катализатора. [24]
В табл. 19 приведены величины энергетических выходов некоторых простых радиационно-химических реакций. Эти данные показывают, что по величине энергетического выхода продуктов реакции радиационно-химические реакции можно подразделить на три группы. Это медленные реакции, характеризующиеся высоким энергетическим барьером, и в некоторых случаях эндотер-мичные. К этой группе относятся, например, реакции азота с водородом и кислородом, разложение воды. В первом случае медленность реакции и связанная с ней малая величина G обусловлены необходимостью активации молекулы азота в каждом акте реакции. [25]
Страницы: 1 2